Dans le test du lysat d’amébocyte de limulus ?
TEST AU LYSAT D’AMEBocyte LIMULUS :
Qu’est-ce que c’est?
Le test de lysat d’amébocytes de limulus est un test sanguin qui mesure le niveau d’un anticorps dans votre sang. Le test est utilisé pour diagnostiquer certains types d’infections, y compris certaines formes de leucémie.
Comment est-il fait?
Le test de lysat d’amébocytes de limulus est généralement effectué dans un hôpital ou un centre médical. Vous recevrez un sédatif avant le test et vous resterez généralement inconscient pendant la procédure. Une fine couche de votre sang sera prélevée de la veine de votre bras. Ce sang sera ensuite mélangé à des cellules spéciales riches en enzymes extraites du muscle du ver rouge de Lima (Limulus polyphemus). Le lysat (l’extrait acellulaire) sera ensuite testé pour la présence d’anticorps contre divers types de cancer et d’autres maladies.
Pourquoi le test de lysat d’amébocytes de limulus est-il utilisé ?
Le test de lysat d’amébocytes de limulus peut être utilisé pour diagnostiquer plusieurs types d’infections, y compris certaines formes de leucémie. La présence d’anticorps contre certains types de cancer ou d’autres maladies peut indiquer que vous avez cette maladie.
Le test au lysat d’amébocyte de limule est un extrait aqueux de cellules sanguines (amoebocytes
amoebocytes
Chez les éponges, les amébocytes, également appelés archéocytes, sont des cellules présentes dans le mésohyle qui peuvent se transformer en n’importe quel type de cellule plus spécialisé de l’animal. Dans la littérature ancienne, le terme amébocyte est parfois utilisé comme synonyme de phagocyte.https://en.wikipedia.org ‘ wiki ‘ Amebocyte
Amebocyte – Wikipédia
) qui obtiennent de la limule ( Limulus polyphemus ). Le test LAL est recommandé dans toutes les pharmacopées internationales comme méthode de recherche des endotoxines bactériennes. Les bactéries Gram-négatives produisent des endotoxines (pyrogènes).
Quel est le but du test des amébocytes de Limulus ?
Le test au lysat d’amoebocyte de Limulus (LAL) est une méthode simple de détection des bactéries Gram-négatives viables et non viables. Certains lipopolysaccharides de la paroi cellulaire (c’est-à-dire les endotoxines) de ce groupe bactérien entraînent la gélification des lysats de cellules sanguines (amoebocytes) du crabe Limulus polyphemus.
Que signifie le terme Limulus dans le test LAL ?
Le lysat d’amébocytes de Limulus (LAL) est un extrait aqueux de cellules sanguines (amibocytes) du crabe Limulus polyphemus de l’Atlantique. Cette réaction est à la base du test LAL, qui est largement utilisé pour la détection et la quantification des endotoxines bactériennes.
Comment extrait-on le lysat de Limulus ?
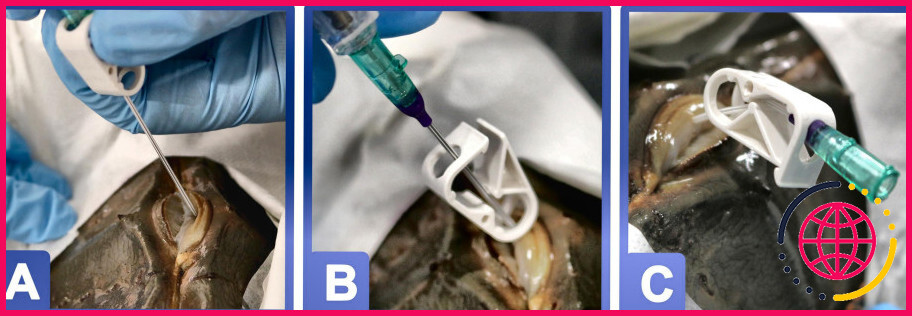
Le lysat est produit en extrayant le sang du crabe. Cela se fait par une méthode non létale où le sang est prélevé dans un grand sinus sanguin dorsal, le péricarde. Les crabes sont remis à l’eau dans les 24 heures et se rétablissent complètement. Jack Levin fait une démonstration du prélèvement de sang sur un Limulus.
Qu’est-ce que lambda dans le test BET ?
Une réponse positive (gel) indique que la quantité d’endotoxine dans l’échantillon atteint ou dépasse la sensibilité étiquetée du réactif, représentée par le symbole lambda, λ. La réaction endotoxine/LAL nécessite un pH neutre et dépend du temps et de la concentration d’endotoxine.
Comment l’endotoxine bactérienne est-elle calculée ?
Pensez-y de la façon suivante :
- Si la dose est de 1 mg/kg/hr, la limite d’endotoxine est de (5 UE/kg/hr) ÷ (1 mg/kg/hr) = 5 UE/mg.
- Si la dose est de 10 mg/kg/h, la limite d’endotoxine est de (5 EU/kg/h) ÷ (10 mg/kg/h) = 0,5 EU/mg.
- Si la dose est de 100mg/kg/hr, la limite d’endotoxine est de (5 EU/kg/hr) ÷ (100 mg/kg/hr) = 0,05 EU/mg.
Comment puis-je réduire mon taux d’endotoxines ?
Les procédures de dépyrogénation les plus courantes pour les composants physiques comprennent l’incinération et l’élimination par lavage, également appelée dilution. La littérature a montré que d’autres procédures, telles que la filtration, l’irradiation et le traitement à l’oxyde d’éthylène, ont un effet limité sur la réduction des niveaux de pyrogènes/endotoxines.
Comment la LAL est-elle extraite ?
Le LAL est dérivé des cellules sanguines, ou amébocytes, de la limule, Limulus polyphemus . Le test de lysat d’amébocyte de Limulus est un extrait aqueux de cellules sanguines (amébocytes) qui obtiennent du crabe des chevaux ( Limulus polyphemus ).
Les limules sont-elles porteuses de maladies ?
Une maladie apparemment courante chez les limules sauvages et captives est une pathologie de la carapace causée par une infection par une algue verte (chlorophycophytal) (figure 1).
Les limules sont-elles en voie de disparition ?
Bien que la limule ne soit pas considérée comme une espèce en danger, sa forte demande a sérieusement diminué le nombre de ses populations, la plaçant sur la liste des « espèces quasi menacées. » Par conséquent, il est illégal dans le New Jersey d’en retirer une de son habitat pour quelque raison que ce soit, mais les lois protégeant les limules…
Qu’est-ce qui n’est pas correct pour le test LAL ?
Erreur n° 1 : faux positifs dus à des polysaccharides fongiques. Le LAL repose sur une réaction de coagulation qui se produit en présence d’endotoxine ; cependant, des études ont montré qu’un polysaccharide fongique appelé (1→3)-β-D-glucan induit également la coagulation, ce qui peut entraîner des résultats faussement positifs.
Qu’est-ce que le lysat d’amibocyte de Limulus et comment est-il utilisé ?
Le lysat d’amibocyte de limule (LAL) est largement utilisé depuis ~30 ans pour la détection de l’endotoxine dans l’assurance qualité des médicaments injectables et des dispositifs médicaux. Le LAL constitue une cascade de protéases à sérine qui sont déclenchées par des traces d’endotoxine, aboutissant à un caillot de gel à la fin de la réaction.
Pourquoi le test LAL est-il si populaire auprès des industries pharmaceutiques ?
L’une des raisons pour lesquelles le test LAL s’est imposé dans l’industrie pharmaceutique est le fait que les fabricants de LAL évitent soigneusement de faire du mal aux animaux vivants, tant pendant la production que pendant les tests. Dans ces cas, le test LAL a permis de réaliser la détection des endotoxines sans aucun problème.
Quel animal est utilisé pour les tests pyrogènes ?
Tests sur les animaux
Dans le test pyrogène du lapin (RPT), qui est utilisé depuis les années 1940, les lapins sont immobilisés et injectés avec une substance à tester tandis que leur température corporelle est surveillée pour détecter les changements qui suggèrent que la substance pourrait être contaminée par des pyrogènes.
Qu’est-ce qui provoque l’endotoxine ?
Source et exposition
L’endotoxine se trouve dans les bactéries Gram-négatives et les produits ou débris bactériens. Ainsi, l’endotoxine est largement présente dans l’environnement, y compris dans la poussière, les déchets animaux, les aliments et d’autres matériaux générés à partir de produits bactériens Gram-négatifs ou exposés à ces derniers.
Qu’est-ce que le test pyrogène du lapin ?
Le test pyrogène a été publié pour la première fois en 1986. Ce test consiste à mesurer les changements de température corporelle des lapins après injection intraveineuse d’une solution stérile de la solution à examiner. Par conséquent, un test couvrant tous les types de pyrogènes est nécessaire pour confirmer l’absence de pyrogènes non endotoxiniques.
La vente de sang de limule est-elle illégale ?
« Cette récolte de limules est illégale et ne devrait pas être autorisée à se poursuivre une année de plus », a déclaré Catherine Wannamaker, avocate principale au Southern Environmental Law Center, dans un communiqué. La limule de l’Atlantique est une espèce protégée et contribue depuis longtemps à la recherche biomédicale.
Les limules sont-elles bonnes à quelque chose ?
Les limules adultes servent de proies aux tortues de mer, aux alligators, aux conques et aux requins. Les limules sont également extrêmement importants pour l’industrie biomédicale car leur sang bleu unique, à base de cuivre, contient une substance appelée « Limulus Amebocyte Lysate », ou « LAL ».
Les limules peuvent-elles vous faire du mal ?
1) Les limules ne piquent pas et ne mordent pas.
Leur queue ne vous fait pas de mal. C’est en fait un moyen qu’ils utilisent pour se redresser, mais dans de nombreux cas, ils s’échouent en haut de la plage pendant la saison du frai. Leur queue peut sembler effrayante mais elle leur sert à s’aider s’ils sont renversés par une vague.
Comment est utilisé Lal ?
Le test LAL (limulus amebocyte lysate), également appelé test d’endotoxine bactérienne, est un test in vitro utilisé pour détecter la présence et la concentration d’endotoxines bactériennes dans les médicaments et les produits biologiques, et constitue une partie importante de la microbiologie pharmaceutique.
Qu’est-ce que le test d’endotoxine bactérienne ?
Le test des endotoxines bactériennes (BET) est un test permettant de détecter ou de quantifier les endotoxines des bactéries Gram- négatif en utilisant un lysat d’amibocyte de la limule (Limulus polyphemus ou. Tachypleus tridentatus).
Qui a découvert Lal ?
Découverte du test LAL (Limulus Amebocyte Lysate). C’est l’histoire de deux hommes remarquables, le Dr Frederik Barry Bang, pionnier de l’application de la biologie marine à la recherche médicale, et Jack Levin, qui a inventé le test LAL au milieu du XXe siècle.
Peut-on filtrer l’endotoxine ?
L’endotoxine est continuellement excrétée par la membrane externe des bactéries gram-négatives viables et est libérée lorsque la cellule bactérienne meurt. Bien que les bactéries soient souvent éliminées en utilisant un filtre de qualité stérilisante de 0,2 μm, le LPS lui-même est difficile à éliminer ou à inactiver car il est extrêmement stable à la chaleur et au pH.
Comment les endotoxines provoquent-elles une inflammation ?
L’endotoxine provoque une activation inflammatoire principalement via l’activation de TLR4 (avec le corécepteur MD2) à la surface des cellules, ce qui entraîne l’activation transcriptionnelle de NF-κB de centaines de gènes inflammatoires, y compris des cytokines pro-inflammatoires telles que TNFα, IL-6 et pro-IL-1β.[4, 17, 18].
Quelles sont les maladies causées par les endotoxines ?
6 Types de maladies chez l’homme liées aux endotoxines des bactéries à Gram négatif.
- Complications liées aux brûlures.
- Maladie des artères coronaires.
- Entérocolite nécrosante néonatale.
- La maladie de Crohn et la colite ulcéreuse.
- La mucoviscidose.
- Maladies auto-immunes.