Qu’est-ce que l’effet bohr et l’effet haldane ?
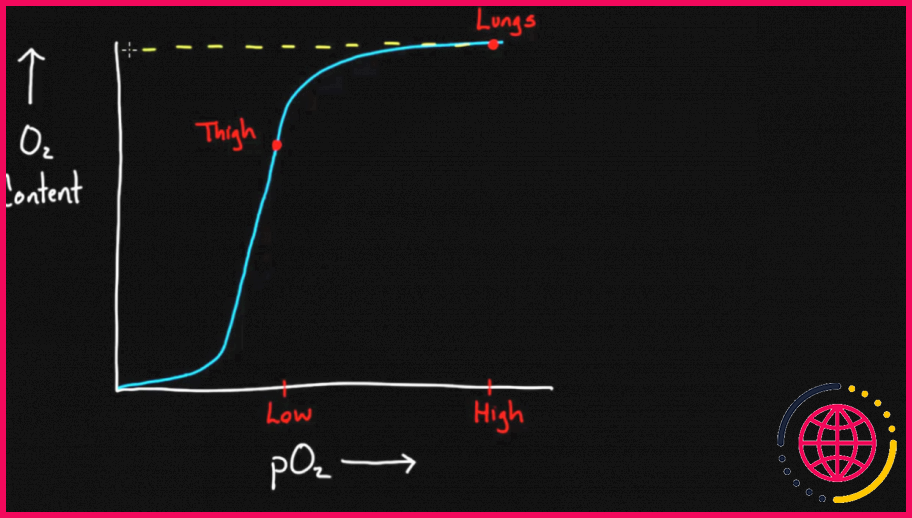
L’effet Bohr et l’effet Haldane dans l’hémoglobine humaine. L’interaction allostérique hétérotrope entre les ligands non héminiques et l’oxygène, collectivement appelée l’effet Bohr , facilite non seulement le transport de l’oxygène mais aussi l’échange de dioxyde de carbone.
En conséquence, on peut aussi se demander ce qu’explique l’effet Bohr ?
Définition de L’effet Bohr . : la diminution de l’affinité pour l’oxygène d’un pigment respiratoire (comme l’hémoglobine) en réponse à la diminution du pH sanguin résultant de l’augmentation de la concentration de dioxyde de carbone dans le sang.
En conséquence, on peut se demander où se produit l’effet Bohr ?
L’effet Bohr fait référence à la perte d’affinité pour l’O2 avec la diminution du pH (augmentation de l’acidité), comme se produit dans la microcirculation lorsque l’oxygène est consommé et que le CO2 (acide carbonique) est libéré par les tissus. Les protons déplacent l’équilibre vers la forme T en se liant aux acides aminés de surface.
En gardant cela à l’esprit, quel est l’effet Haldane dans la respiration ?
L’effet Haldane est une propriété de l’hémoglobine décrite pour la première fois par John Scott Haldane . L’oxygénation du sang dans les poumons déplace le dioxyde de carbone de l’hémoglobine, ce qui augmente l’élimination du dioxyde de carbone. Cette propriété est l’effet Haldane . Par conséquent, le sang oxygéné a une affinité réduite pour le dioxyde de carbone.
Qu’est-ce que l’effet Haldane quizlet ?
Facilite l’échange réciproque d’oxygène pour le dioxyde de carbone. quel est le double effet Haldane ? Au fur et à mesure de l’absorption d’oxygène par le sang fœtal, la libération de dioxyde de carbone devient plus probable. Le double effet Haldane représente environ 46% du transfert transplacentaire de dioxyde de carbone.
Pourquoi l’effet Bohr est-il important ?
L’ effet Bohr permet une décharge accrue d’oxygène dans les tissus périphériques métaboliquement actifs tels que les muscles squelettiques en exercice. L’augmentation de l’activité des muscles squelettiques entraîne des augmentations localisées de la pression partielle du dioxyde de carbone qui, à son tour, réduit le pH sanguin local.
Qu’est-ce que l’effet Bohr et comment fonctionne-t-il ?
L’ effet Bohr décrit la capacité des globules rouges à s’adapter aux changements de l’environnement biochimique, en maximisant la capacité de liaison hémoglobine-oxygène dans les poumons tout en optimisant simultanément l’apport d’oxygène aux tissus les plus sollicités.
Pourquoi la myoglobine ne présente-t-elle pas l’effet Bohr ?
L’ effet Bohr est la baisse de la saturation de l’hémoglobine qui se produit avec une diminution du pH et la liaison du CO2 aux groupes N- terminaux -NH2. La myoglobine ne présente pas d’effet Bohr car elle ne possède pas de structure quaternaire permettant de réguler le degré de saturation par l’O2.
Quelle est la signification de pCO2 ?
pression partielle du dioxyde de carbone.
Comment le pH affecte-t-il l’hémoglobine ?
Transport de l’oxygène
Lorsque le sang s’approche des poumons, la concentration en dioxyde de carbone diminue, entraînant une augmentation de la pH . Cette augmentation de la pH augmente l’affinité de l’ hémoglobine pour l’oxygène par le biais de l’ effet Bohr , ce qui fait que l’ hémoglobine capte l’oxygène qui entre dans votre sang depuis vos poumons afin de le transporter vers vos tissus.
L’hémoglobine transporte-t-elle du co2 ?
Hémoglobine : La protéine à l’intérieur des globules rouges (a) qui transporte l’oxygène aux cellules et le dioxyde de carbone aux poumons est l’ hémoglobine (b). L’hémoglobine est constituée de quatre sous-unités symétriques et de quatre groupes hèmes. Cela s’explique par le fait que la molécule d’ hémoglobine change de forme, ou de conformation, lorsque l’oxygène se fixe.
Qu’est-ce que l’effet Bohr dans l’hémoglobine ?
L’ effet Bohr a été découvert pour la première fois par un physiologiste Christian Bohr en 1904. Cet effet explique comment les ions hydrogène et le dioxyde de carbone affectent l’affinité de l’oxygène dans l’ Hémoglobine . Si le pH était inférieur à ce qu’il était normalement (le pH physiologique normal est de 7,4), alors la hémoglobine ne fixe pas aussi bien l’oxygène.
Qu’est-ce que la carboxyhémoglobinémie ?
Carboxyhémoglobinémie : Présence de carboxyhémoglobine dans le sang. La carboxyhémoglobine , hémoglobine à laquelle est lié du monoxyde de carbone, se forme lors d’une intoxication au monoxyde de carbone, par exemple à partir des gaz d’échappement (d’une voiture, d’un camion, d’un bateau ou d’un générateur), de la fumée d’un incendie ou de la fumée de tabac.
Pourquoi l’hémoglobine est-elle un tampon ?
Les systèmes tampon protéiques dépendent des protéines, par opposition aux molécules non protéiques, pour agir comme des tampons et consommer de petites quantités d’acide ou de base. La protéine hémoglobine fait un excellent tampon . Elle peut se lier à de petites quantités d’acide dans le sang, aidant à éliminer cet acide avant qu’il ne modifie le pH du sang.
Comment l’hémoglobine libère-t-elle l’oxygène ?
L’hémoglobine libère l’ oxygène lié lorsque l’acide carbonique est présent, comme c’est le cas dans les tissus. Dans les capillaires, où le dioxyde de carbone est produit, l’ oxygène lié à l’ hémoglobine est libéré dans le plasma du sang et absorbé dans les tissus.
Comment la température affecte-t-elle l’hémoglobine ?
Il s’avère que la température affecte l’affinité, ou la force de liaison, de l’ hémoglobine pour l’oxygène. Plus précisément, l’augmentation de la température diminue l’affinité de l’ hémoglobine pour l’oxygène. Lorsque l’oxyhémoglobine est exposée à des températures plus élevées dans les tissus en cours de métabolisation, l’affinité diminue et la hémoglobine se décharge de l’oxygène.
Comment les 2/3 bpg affectent-ils l’hémoglobine ?
L’accumulation de 2 , 3 – BPG diminue l’affinité de l’hémoglobine pour l’oxygène. Dans les tissus à forte demande énergétique, l’oxygène est rapidement consommé, ce qui augmente la concentration de H+ et de dioxyde de carbone. Grâce à l’ effet Bohr , l’ hémoglobine est incitée à libérer plus d’oxygène pour alimenter les cellules qui en ont besoin.
Pourquoi l’oxygène est-il mauvais pour la BPCO ?
Chez les personnes atteintes de bronchopneumopathie chronique obstructive et de problèmes pulmonaires similaires, les caractéristiques cliniques de la toxicité de l’ oxygène sont dues à une teneur élevée en dioxyde de carbone dans le sang (hypercapnie). Cela entraîne une somnolence (narcose), un dérèglement de l’équilibre acido-basique dû à une acidose respiratoire, et la mort.
Comment le dioxyde de carbone est-il transporté dans le sang ?
Les molécules de dioxyde de carbone sont transportées dans le sang des tissus corporels vers les poumons par l’une des trois méthodes suivantes : dissolution directement dans le sang , liaison à l’hémoglobine, ou transport sous forme d’ion bicarbonate. Deuxièmement, le dioxyde de carbone peut se lier aux protéines plasmatiques ou peut pénétrer dans les sang rouges et se lier à l’hémoglobine.
Qu’est-ce que la courbe de réponse du co2 ?
La courbe de réponse au dioxyde de carbone représente une partie essentielle de cette boucle de rétroaction négative des chimiorécepteurs, s’appuyant sur les chimiorécepteurs centraux et périphériques pour détecter les altérations de l’équilibre acide/base, modifiant finalement notre pulsion respiratoire pour maintenir l’homéostasie.
Quels sont les gaz respiratoires ?
Trois gaz respiratoires vitaux – l’oxygène (O(2)), le monoxyde d’azote (NO) et le dioxyde de carbone (CO(2)) – se croisent au niveau du globule rouge (GR) humain.
Qu’est-ce que la rétention de co2 ?
L’hypercapnie est une accumulation excessive de dioxyde de carbone ( CO2 ) dans votre corps. Cet état, également décrit comme une hypercapnie, une hypercarbie ou une rétention de dioxyde de carbone , peut provoquer des effets tels que des maux de tête, des vertiges et de la fatigue, ainsi que des complications graves telles que des crises ou une perte de conscience.
Lorsque le sang s'approche des poumons, la concentration en dioxyde de carbone diminue, entraînant une augmentation de la pH. Cette augmentation de la pH augmente l'affinité de l'hémoglobine pour l'oxygène par le biais de l'effet Bohr, ce qui fait que l'hémoglobine capte l'oxygène qui entre dans votre sang depuis vos poumons afin de le transporter vers vos tissus." } }, {"@type": "Question","name": " L'hémoglobine transporte-t-elle du co2 ? ","acceptedAnswer": {"@type": "Answer","text": " Hémoglobine : La protéine à l'intérieur des globules rouges (a) qui transporte l'oxygène aux cellules et le dioxyde de carbone aux poumons est l' hémoglobine (b). L'hémoglobine est constituée de quatre sous-unités symétriques et de quatre groupes hèmes. Cela s'explique par le fait que la molécule d'hémoglobine change de forme, ou de conformation, lorsque l'oxygène se fixe." } }, {"@type": "Question","name": " Qu'est-ce que l'effet Bohr dans l'hémoglobine ? ","acceptedAnswer": {"@type": "Answer","text": " L'effet Bohr a été découvert pour la première fois par un physiologiste Christian Bohr en 1904. Cet effet explique comment les ions hydrogène et le dioxyde de carbone affectent l'affinité de l'oxygène dans l'Hémoglobine. Si le pH était inférieur à ce qu'il était normalement (le pH physiologique normal est de 7,4), alors la hémoglobine ne fixe pas aussi bien l'oxygène." } }, {"@type": "Question","name": " Qu'est-ce que la carboxyhémoglobinémie ? ","acceptedAnswer": {"@type": "Answer","text": " Carboxyhémoglobinémie : Présence de carboxyhémoglobine dans le sang. La carboxyhémoglobine, hémoglobine à laquelle est lié du monoxyde de carbone, se forme lors d'une intoxication au monoxyde de carbone, par exemple à partir des gaz d'échappement (d'une voiture, d'un camion, d'un bateau ou d'un générateur), de la fumée d'un incendie ou de la fumée de tabac.
" } }, {"@type": "Question","name": " Pourquoi l'hémoglobine est-elle un tampon ? ","acceptedAnswer": {"@type": "Answer","text": " Les systèmes tampon protéiques dépendent des protéines, par opposition aux molécules non protéiques, pour agir comme des tampons et consommer de petites quantités d'acide ou de base. La protéine hémoglobine fait un excellent tampon. Elle peut se lier à de petites quantités d'acide dans le sang, aidant à éliminer cet acide avant qu'il ne modifie le pH du sang." } }, {"@type": "Question","name": " Comment l'hémoglobine libère-t-elle l'oxygène ? ","acceptedAnswer": {"@type": "Answer","text": " L'hémoglobine libère l'oxygène lié lorsque l'acide carbonique est présent, comme c'est le cas dans les tissus. Dans les capillaires, où le dioxyde de carbone est produit, l'oxygène lié à l'hémoglobine est libéré dans le plasma du sang et absorbé dans les tissus." } }, {"@type": "Question","name": " Comment la température affecte-t-elle l'hémoglobine ? ","acceptedAnswer": {"@type": "Answer","text": " Il s'avère que la température affecte l'affinité, ou la force de liaison, de l'hémoglobine pour l'oxygène. Plus précisément, l'augmentation de la température diminue l'affinité de l'hémoglobine pour l'oxygène. Lorsque l'oxyhémoglobine est exposée à des températures plus élevées dans les tissus en cours de métabolisation, l'affinité diminue et la hémoglobine se décharge de l'oxygène." } }, {"@type": "Question","name": " Comment les 2/3 bpg affectent-ils l'hémoglobine ? ","acceptedAnswer": {"@type": "Answer","text": " L'accumulation de 2,3-BPG diminue l'affinité de l'hémoglobine pour l'oxygène. Dans les tissus à forte demande énergétique, l'oxygène est rapidement consommé, ce qui augmente la concentration de H+ et de dioxyde de carbone. Grâce à l'effet Bohr, l'hémoglobine est incitée à libérer plus d'oxygène pour alimenter les cellules qui en ont besoin." } }, {"@type": "Question","name": " Pourquoi l'oxygène est-il mauvais pour la BPCO ? ","acceptedAnswer": {"@type": "Answer","text": " Chez les personnes atteintes de bronchopneumopathie chronique obstructive et de problèmes pulmonaires similaires, les caractéristiques cliniques de la toxicité de l'oxygène sont dues à une teneur élevée en dioxyde de carbone dans le sang (hypercapnie). Cela entraîne une somnolence (narcose), un dérèglement de l'équilibre acido-basique dû à une acidose respiratoire, et la mort." } }, {"@type": "Question","name": " Comment le dioxyde de carbone est-il transporté dans le sang ? ","acceptedAnswer": {"@type": "Answer","text": " Les molécules de dioxyde de carbone sont transportées dans le sang des tissus corporels vers les poumons par l'une des trois méthodes suivantes : dissolution directement dans le sang, liaison à l'hémoglobine, ou transport sous forme d'ion bicarbonate. Deuxièmement, le dioxyde de carbone peut se lier aux protéines plasmatiques ou peut pénétrer dans les sang rouges et se lier à l'hémoglobine." } }, {"@type": "Question","name": " Qu'est-ce que la courbe de réponse du co2 ? ","acceptedAnswer": {"@type": "Answer","text": " La courbe de réponse au dioxyde de carbone représente une partie essentielle de cette boucle de rétroaction négative des chimiorécepteurs, s'appuyant sur les chimiorécepteurs centraux et périphériques pour détecter les altérations de l'équilibre acide/base, modifiant finalement notre pulsion respiratoire pour maintenir l'homéostasie." } }, {"@type": "Question","name": " Quels sont les gaz respiratoires ? ","acceptedAnswer": {"@type": "Answer","text": " Trois gaz respiratoires vitaux - l'oxygène (O(2)), le monoxyde d'azote (NO) et le dioxyde de carbone (CO(2)) - se croisent au niveau du globule rouge (GR) humain." } }] }