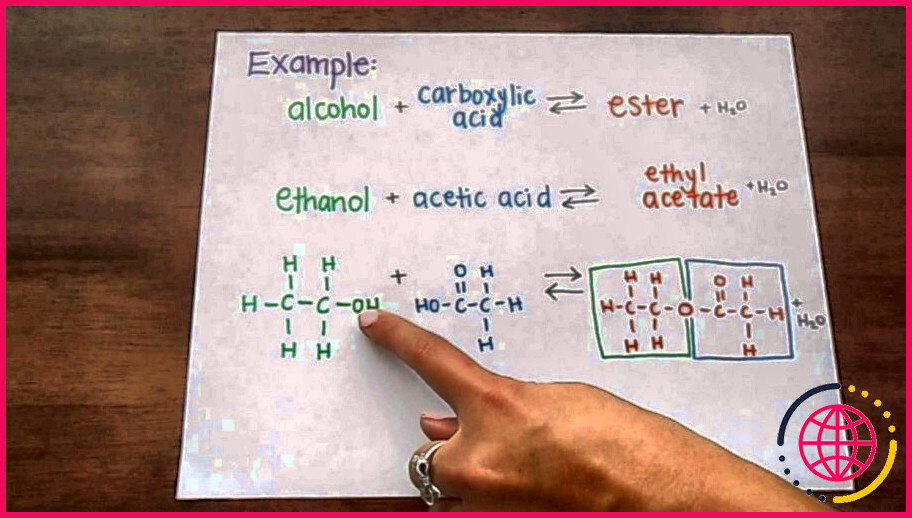
Comment fait-on l’estérification ?
Le processus d’ estérification
L’estérification se produit lorsqu’un acide carboxylique réagit avec un alcool. Cette réaction peut se produire uniquement en présence d’un catalyseur acide et de chaleur. Il faut beaucoup d’énergie pour enlever le -OH de l’acide carboxylique, donc un catalyseur et la chaleur sont nécessaires pour produire l’énergie nécessaire.
Il faut aussi savoir comment on fait les réactions d’estérification.
Pour faire un petit ester comme l’éthanoate d’éthyle, on peut chauffer doucement un mélange d’acide éthanoïque et d’éthanol en présence d’acide sulfurique concentré, et distiller l’ ester dès qu’il est formé. Cela évite que la réaction inverse ne se produise.
De même, comment identifier l’estérification ? Les esters sont nommés comme si la chaîne alkyle de l’alcool était un substituant.
Les esters peuvent être nommés en utilisant quelques étapes
- Premièrement, identifier l’oxygène qui fait partie de la chaîne continue et qui est lié au carbone des deux côtés.
- Deuxièmement, commencez à numéroter les chaînes de carbone de part et d’autre de l’oxygène identifié à l’étape 1.
À cet égard, quel est le processus d’estérification ?
L’estérification est une réaction chimique qui forme au moins un ester (= un type de composé produit par réaction entre des acides et des alcools). Les esters sont produits lorsque des acides sont chauffés avec des alcools dans un processus appelé estérification . Un ester peut être fabriqué par une réaction d’ estérification d’un acide carboxylique et d’un alcool.
Qu’est-ce que l’estérification donnez un exemple ?
Certains esters peuvent être préparés par estérification , une réaction dans laquelle un acide carboxylique et un alcool, chauffés en présence d’un catalyseur acide minéral, forment un ester et de l’eau : La réaction est réversible. Comme exemple spécifique d’une réaction d’ estérification , l’acétate de butyle peut être fabriqué à partir d’acide acétique et de 1-butanol.
Le COOH est-il un acide ou une base ?
Les groupes carboxyles sont des acides faibles, se dissociant partiellement pour libérer des ions hydrogène. Le groupe carboxyle (symbolisé par COOH ) a à la fois un groupe carbonyle et un groupe hydroxyle attachés au même atome de carbone, ce qui entraîne de nouvelles propriétés.
L’estérification est-elle sn1 ou sn2 ?
Oui. L’estérification sera certainement une réaction bimoléculaire parce que le groupe OH serait peu susceptible de se dissocier et de former un carbocation pour les raisons que vous avez énoncées ci-dessus. Maintenant, le mécanisme est légèrement différent de la réaction standard SN2 qui procède par la formation d’un état de transition pentavalent.
Les esters sont-ils solubles dans l’eau ?
Solubilité dans l’eau
Les petits esters sont assez solubles dans l’eau mais la solubilité diminue avec la longueur de la chaîne. La raison de cette solubilité est que, bien que les esters ne puissent pas se lier par hydrogène avec eux-mêmes, ils peuvent se lier par hydrogène avec les molécules d’ eau .
À quoi sert l’estérification ?
Le procédé d’ estérification continue est utilisé industriellement pour fabriquer de l’acétate de méthyle à partir d’acide acétique et de méthanol et de l’acétate d’éthyle à partir d’acide acétique et d’éthanol. Le procédé alternatif consistant à fabriquer des esters à partir de la réaction d’un alcool avec un anhydride est important dans la fabrication de médicaments.
Pourquoi l’estérification est-elle lente ?
On fait souvent chauffer ensemble des acides carboxyliques et des alcools en présence de quelques gouttes d’acide sulfurique concentré afin d’observer l’odeur des esters formés. Comme les réactions sont lentes et réversibles, on n’obtient pas beaucoup d’ esters produits pendant ce temps.
Pourquoi l’estérification se fait-elle sous reflux ?
Le chauffage du mélange réactionnel sous reflux évite la perte de réactifs et de produits volatils. L’acide sulfurique concentré est utilisé comme catalyseur pour accélérer la vitesse de formation de l’ester (6).
Le phénol est-il un alcool ?
phénols . Un phénol est constitué d’un -OH lié à un carbone sp2 insaturé. Il n’est donc pas qualifié d’ alcool .
Quelle est l’odeur des esters ?
Esters . Les esters sont des molécules polaires, mais leurs points d’ébullition sont plus bas que ceux des acides carboxyliques et des alcools de poids moléculaire similaire parce qu’il n’y a pas de liaison hydrogène intermoléculaire entre les molécules d’ ester . Les acides ont des odeurs désagréables, mais les esters ont des fruits .
odeurs.
Quel est le contraire de l’estérification ?
L’hydrolyse acide est simplement l’ inverse de l’estérification . L’ ester est chauffé avec un grand excès d’eau contenant un catalyseur acide fort. Comme l’ estérification , la réaction est réversible et ne va pas jusqu’à son terme.
Que sont les réactions d’estérification ?
L’estérification est une réaction chimique qui forme au moins un ester (= un type de composé produit par réaction entre des acides et des alcools). Les esters sont produits lorsque des acides sont chauffés avec des alcools dans un processus appelé estérification . Un ester peut être fabriqué par une réaction d’estérification d’un acide carboxylique et d’un alcool.
Pourquoi cela s’appelle-t-il estérification ?
L’estérification est le nom général d’une réaction chimique dans laquelle deux réactifs (généralement un alcool et un acide) forment un ester comme produit de réaction.
Quelle est la première étape d’une réaction d’estérification ?
Dans la première étape, l’ acide éthanoïque prend un proton (un ion hydrogène) à partir de l’ acide sulfurique concentré. Le proton se fixe sur l’une des paires solitaires de l’oxygène qui est doublement lié au carbone.
Quelle est la différence entre estérification et transestérification ?
L’estérification est la réaction entre un acide carboxylique et un alcool alors que la transestérification se produit entre un ester et un alcool.
Combien de temps dure l’estérification ?
Les temps de réaction typiques varient de 1 à 10 heures à des températures de 60 à 110 °C. Les acylations directes d’alcools avec des acides carboxyliques sont préférées aux acylations avec des anhydrides (mauvaise économie d’atomes) ou des chlorures d’acides (sensibles à l’humidité).
L’estérification est-elle une réaction de déshydratation ?
Réactions de déshydratation
L’exemple classique d’une réaction de déshydratation est la estérification de Fischer, qui consiste à traiter un acide carboxylique avec un alcool en présence d’un agent déshydratant : Dans la réaction de condensation qui lui est liée, l’eau est libérée de deux réactifs différents.
L’estérification est-elle exothermique ou endothermique ?
Le processus d’estérification peut être classé comme une réaction exothermique où dans chaque réaction ; quelques quantités de chaleur seront libérées dans l’environnement. De là, c’est une réaction assez simple ; l’étude sur les dégagements de chaleur ne doit pas être exceptionnelle.
Comment faire la différence entre un acide carboxylique et un ester ?
Les acides carboxyliques donnent une couleur rouge vin par réaction avec du FeCl3 neutre fraîchement préparé alors que les esters ne le font pas. Le test de l’effervescence peut également être effectué avec du carbonate ou du bicarbonate de sodium qui est négatif pour les esters . Une autre méthode est simplement l’épreuve de lithmus car les acides carboxyliques virent au bleu de litmus alors que les esters ne le font pas.