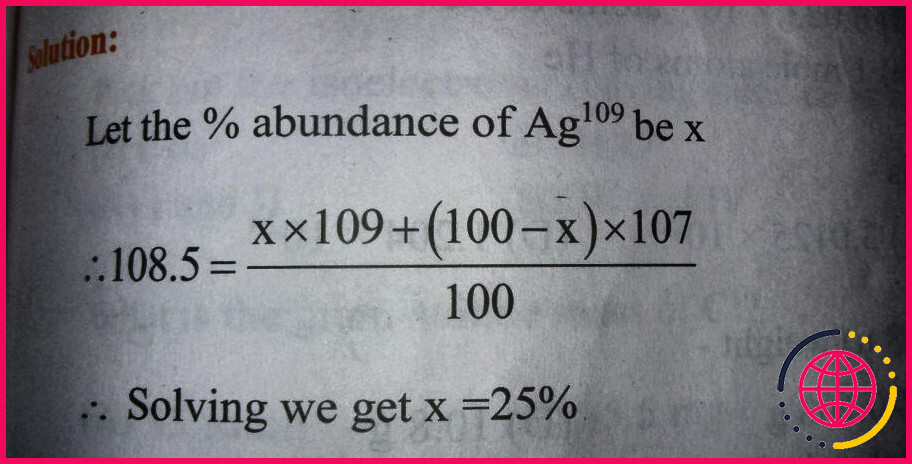Comment trouver la masse de l’ag 109 ?
Si l’argent est composé à 51,84% de Ag -107 avec une masse de 106,9051 amu et le reste de Ag – 109 avec une masse de 108,9048 amu, calculez la masse atomique de l’argent .
Savoir aussi, quelle est la masse de Ag – 109?
Question : L’argent a une masse atomique de 107,868 amu et seulement deux isotopes naturels. L’isotope Ag – 109 (108,905 amu) a une abondance naturelle de 48,16%.
A part ce qui précède, combien d’électrons possède AG 109 ?
protons = 47 électrons = 47 neutrons = 60 b. Comment les nombres de protons, neutrons et électrons dans un atome neutre de Ag-109 se comparent-ils à ceux de Ag-107 ? Ag-109 et Ag-107 ont tous deux le même nombre d’électrons et de protons. Cependant, l’Ag-109 possède deux neutrons supplémentaires.
De plus, comment trouver la masse moyenne d’un isotope ?
Pour calculer la masse moyenne , il faut d’abord convertir les pourcentages en fractions (les diviser par 100). Ensuite, calculez les nombres de masse . Le chlore isotope à 18 neutrons a une abondance de 0,7577 et un nombre masse de 35 amu.
Qu’est-ce qui a une masse de 1 amu ?
Une unité de masse atomique (symbolisée UMA ou amu) est définie comme étant précisément 1/12 de la masse d’un atome de carbone-12. L’atome de carbone-12 (C-12) possède six protons et six neutrons dans son noyau. En termes imprécis, une UAM est la moyenne de la masse au repos du proton et de la masse au repos du neutron .
Quelle est la masse atomique de l’Ag ?
107.8682 u
Comment trouve-t-on le nombre de masse ?
Ensemble, le nombre de protons et le nombre de neutrons déterminent le nombre de masse d’un élément : nombre de masse = protons + neutrons. Si vous voulez calculer le nombre de neutrons d’un atome, vous pouvez simplement soustraire le nombre de protons, ou nombre atomique, du nombre de masse .
Quelle est la masse atomique du néon 22 ?
Les derniers 8,85% des atomes sont des Ne- 22 , qui est un isotope du néon avec 12 neutrons et une masse de 21,99amu.
Comment détermine-t-on les isotopes ?
Soustrayez le numéro atomique (le nombre de protons) du poids atomique arrondi. Cela vous donne le nombre de neutrons dans l’ isotope le plus commun. Utilisez le tableau périodique interactif du projet Isotopes du laboratoire Berkeley pour trouver quels autres isotopes de cet élément existent.
Comment trouver la masse moyenne en chimie ?
La masse atomique moyenne d’un élément est calculée en additionnant les masses des isotopes de l’élément, chacune multipliée par son abondance naturelle sur Terre. Lors de tout calcul de masse impliquant des éléments ou des composés, il faut toujours utiliser la masse atomique moyenne, que l’on trouve sur le tableau périodique.
Pourquoi les masses atomiques ne sont-elles pas des nombres entiers ?
La masse atomique n’est jamais un nombre entier pour plusieurs raisons : La masse atomique rapportée sur un tableau périodique est la moyenne pondérée de tous les isotopes existant à l’état naturel. S’agissant d’une moyenne, il serait très improbable qu’elle soit un nombre entier . La masse d’un atome individuel en unités de masse atomique est la masse relative au carbone-12.
Qu’est-ce que la masse atomique quizlet ?
Qu’est-ce que la masse atomique ? La somme de tous les protons et neutrons du noyau atomique .
Comment calculer la masse atomique de l’oxygène ?
15.999 u
En quoi la masse atomique moyenne est-elle différente du numéro de masse ?
La masse atomique est la masse moyenne pondérée d’un atome d’un élément en fonction de l’abondance naturelle relative des isotopes de cet élément. Le nombre de masse est un compte du nombre total de protons et de neutrons dans le noyau d’un atome .
Qu’est-ce que la masse molaire en chimie ?
La masse molaire est la masse d’un élément chimique ou d’un composé chimique donné (g) divisé par la quantité de substance (mol). La masse molaire d’un composé peut être calculée en additionnant les masses atomiques standard (en g/mol) des atomes constitutifs.
Combien d’électrons y a-t-il dans ag ?
47 électrons.
Comment le calcium obéit-il à la règle de l’octuor ?
Calcium
, Ca , est situé dans le groupe 2 du tableau périodique, ce qui signifie qu’il possède deux électrons sur sa coquille la plus externe. Afin d’avoir un octet complet, le calcium doit perdre ces deux électrons les plus à l’extérieur, également appelés électrons de valence. Le calcium réagira avec des non-métaux pour former des composés ioniques.
Quelle est la masse atomique de l’argent ?
107.8682 u
Combien de neutrons y a-t-il dans l’ag ?
L’argent est le deuxième élément de la onzième colonne du tableau périodique. Il est classé comme un métal de transition. Les atomes d’argent ont 47 électrons et 47 protons avec 60 neutrons dans l’isotope le plus abondant.
Quel est le nombre de masse de 108ag ?
Argent-108
| PubChem CID: | 167088 |
|---|---|
| Structure: | Recherche de structures similaires |
| Formule moléculaire: | Ag |
| Synonymes: | 14391-65-2 Argent-108 Argent, isotope de masse 108Ag Argent 108 Plus |
| Poids moléculaire: | 107,90595 g/mol |
Combien de neutrons y a-t-il dans 107 Ag ?
60 neutrons
Comment trouvez-vous les électrons ?
Le nombre d’ électrons dans un atome neutre est égal au nombre de protons. Le nombre de masse de l’atome (M) est égal à la somme du nombre de protons et de neutrons dans le noyau. Le nombre de neutrons est égal à la différence entre le nombre de masse de l’atome (M) et le numéro atomique (Z).