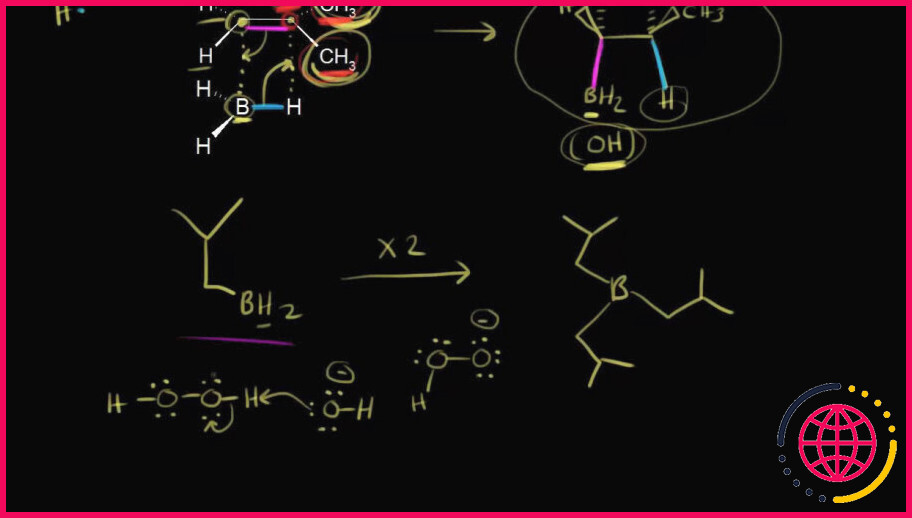
Pourquoi le bh3 est-il réactif ?
L’atome de bore dans BH3 a 6 électrons de valence. Par conséquent, il est un acide de Lewis fort et réagit avec n’importe quelle base de Lewis, L pour former un adduit. dans lequel la base donne sa paire solitaire, formant une liaison covalente dative. De tels composés sont thermodynamiquement stables, mais peuvent être facilement oxydés à l’air.
Ici, pourquoi le bh3 est-il si réactif ?
L’atome de bore dans BH3 possède 6 électrons de valence. Par conséquent, il est un acide de Lewis fort et réagit avec n’importe quelle base de Lewis, L pour former un adduit. dans lequel la base donne sa paire solitaire, formant une liaison covalente dative. De tels composés sont thermodynamiquement stables, mais peuvent être facilement oxydés à l’air.
On peut également se demander pourquoi le borane est réactif ? parce qu’il est très réactif par rapport à la plupart des autres substrats avec des liaisons C-H. La gamme des moins réactifs phosphine- boranes aux plus réactifs pyridine- borane est un facteur d’environ 40.
.
On peut également se demander ce que fait le bh3 dans une réaction ?
L’utilisation la plus importante du BH3 est l’hydroboration des alcènes et des alcynes. Pour la réaction des alcènes, il y a deux choses importantes à garder à l’esprit. La réaction est sélective pour l’alcool le moins substitué (régiosélective). On parle généralement de sélectivité « anti-Markovnikoff ».
Le bh3 est-il un agent réducteur ?
Complexes de borane : BH3 -L Borane est couramment utilisé pour la réduction des acides carboxyliques en présence d’esters, de lactones, d’amides, d’halogénures et d’autres groupes fonctionnels. En outre, le borane réduit rapidement les aldéhydes, les cétones et les alcènes.
Le bh3 est-il un électrophile ?
BH3 n’est pas un nucléophile. C’est un électrophile en raison des orbitales p vides. Voir l’image pour une représentation graphique. Un nucléophile ajouterait ses électrons dans l’orbitale p vide (ce qui signifie que le borane est un acide de Lewis).
Comment s’appelle le bh3 ?
7.11 – Les hydrures moléculaires du bore sont appelés boranes. On les nomme en citant le nombre d’atomes de bore dans la molécule comme préfixe numérique au terme borane (sauf pour le préfixe mono- qui est omis, BH3 étant nommé borane ).
Le bh3 est-il polaire ou non polaire ?
La molécule NH3 résultante est polaire . Chaque liaison B-H dans BH3 est polaire / forme un dipôle car les atomes B et H ont des électronégativités différentes. La forme de la molécule est un plan trigonal qui est symétrique, donc les dipôles / polarités des liaisons s’annulent. La molécule BH3 résultante est non polaire .
Le bh3 est-il soluble dans l’eau ?
L’ammoniac borane est une source potentielle de combustible d’hydrogène en raison de son pourcentage élevé (par poids moléculaire) d’hydrogène. Il a la formule chimique de NH3 BH3 . Il est également soluble dans l’éther et l’eau tout en ne réagissant pas.
Le bh3 existe-t-il ?
Explication : La molécule Bh3 est une molécule déficiente en électrons dans la nature puisque les 6 électrons sont autour de l’atome ‘B’. Le Bf3 est également déficient mais en raison de la plus grande taille de l’atome ‘F’, il ne peut pas subir de dimérisation, donc il existe sous forme de Bf3 avec une charge négative partielle dans le bore et une charge positive partielle sur le fluor.
Le borane est-il un acide de Lewis ?
1 : Borane est un acide de Lewis . Il peut accepter des électrons d’un atome donneur. Le carré dessiné à côté du bore est utilisé pour renforcer l’idée qu’il y a un site vacant pour les électrons à cet endroit. Les acides de Lewis sont souvent à court d’un octuor complet.
Est-ce que bh3 est un hydrure ?
Pourquoi BH3 son classé comme un » Hydrure moléculaire » et AlH3 son un » Hydrure intermédiaire ». Tout d’abord, je comprends que, sur BH3, la différence d’élétronegativité entre B et H est très faible. Ce qui signifie que la liaison B-H est moins polarisée.
Le bf3 se dissoudra-t-il dans l’eau ?
Le trifluorure de bore est le composé inorganique de formule BF3 . Il se dissout rapidement dans l’ eau et dans tout composé organique contenant de l’azote ou de l’oxygène. Il peut être lentement hydrolysé par l’ eau froide pour donner de l’acide fluorhydrique, et peut également s’hydrolyser pour former des fumées blanches et denses dans l’air humide.
Le bh3 est-il un markovnikov ?
BH3 – THF est le même que BH3 . Tétrahydrofurane ( THF ) est simplement un solvant. On écrit parfois B2H6, qui est une autre forme de BH3 . Il s’agit de réactifs d’hydroboration dans lesquels deux des atomes H de BH3 ont été remplacés par des atomes de carbone.
Pourquoi le bh3 est anti markovnikov ?
La première étape est l’attaque de l’alcène sur BH3 , qui forme alors un intermédiaire cyclique à quatre chaînons de liaisons partielles. C’est grâce à cet intermédiaire que l’hydroboration forme le produit anti – Markovnikov . L’atome de bore est hautement électrophile en raison de son orbitale p vide (ie.
.
Quelles sont les réactions qui sont anti markovnikov ?
Anti-Markovnikov addition : Dans une réaction d’addition d’un électrophile générique HX à un alcène ou un alcyne, l’atome d’hydrogène de HX devient lié à l’atome de carbone qui avait le moins d’atomes d’hydrogène dans l’alcène ou l’alcyne de départ.
Que fait le NaOH en tant que réactif ?
Le réactif hydroxyde de sodium ( NaOH ) L’hydroxyde de sodium est largement utilisé en biochimie. C’est une solution basique et a la capacité d’augmenter le pH des solutions chimiques, par exemple il est utile pour la neutralisation des acides.
Pourquoi le THF est-il utilisé dans l’hydroboration ?
Borane est un acide de Lewis parce qu’il a orbitale vacante. et borane est très réactif chimique et a pris le feu dans l’air et facilement réagir avec l’eau. Donc une base de Lewis THF est utilisée comme solvant. Le THF de l’atome d’oxygène donne sa paire solitaire au borane.
L’hydroboration est-elle un synonyme ?
L’hydroboration se déroule de manière antimarkovnikov. La séquence réactionnelle est également stéréospécifique, donnant une addition syn (sur la même face de l’alcène) : l’ hydroboration est syn -sélective et l’oxydation remplace le bore par un hydroxyle ayant la même position géométrique.
A quoi sert le 9 BBN ?
Ce réactif solide incolore est utilisé comme un agent hydroborant très sélectif et stable ; hydratation anti-Markovnikov des alcènes et des alcynes. 9 – BBN -H réduit sélectivement les chlorures d’acide, les aldéhydes, les cétones, les lactones et les sulfoxydes à 25 °C.
Qu’est-ce qu’une réaction régiosélective ?
La régiosélectivité est la préférence d’une direction de création ou de rupture de liaison chimique par rapport à toutes les autres directions possibles. La régiosélectivité peut aussi s’appliquer à des réactions spécifiques comme l’addition à des ligands pi. La sélectivité se produit également dans les insertions de carbènes, par exemple dans la réaction de Baeyer-Villiger.
Que font h2o2 et NaOH dans une réaction ?
Le mélange de hydroxyde de sodium et de peroxyde d’hydrogène produit un oxydant fort appelé peroxyde de sodium et peut entraîner un brouillard exothermique à partir de l’apparition de températures élevées et de la chaleur provenant de la décomposition de mélanges incompatibles causant un danger thermique grave. (2 NaOH + H2O2 →Na2O2 + 2 H2O).