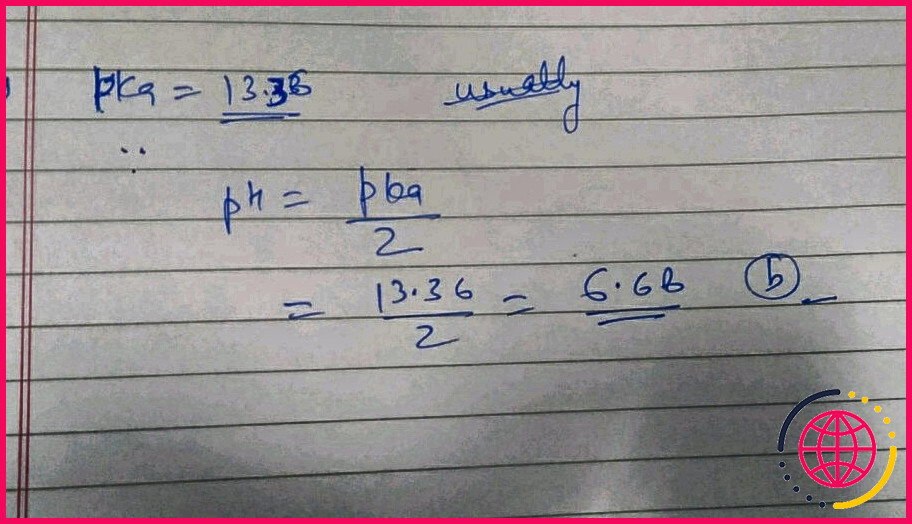Quel est le ph de l’eau pure à 50 c ?
Cette question est en fait trompeuse ! En fait, l’ eau pure n’a un pH de 7 qu’à une température particulière – celle à laquelle la valeur de Kw est de 1,00 x 10–14 mol2 dm–6.
| T (° C ) | Kw (mol2 dm–6) | pH |
|---|---|---|
| 25 | 1,008 x 10–14 | 7,00 |
| 30 | 1,471 x 10–14 | 6,92 |
| 40 | 2,916 x 10–14 | 6,77 |
| 50 | 5. 476 x 10–14 | 6,63 |
Aussi demandé, quel est le pH de l’eau pure à cette température ?
A la température ambiante (25 degrés Celsius), le pH de l’eau pure est de 7. Si vous augmentez la température à 100 degrés Celsius, le pH de l’eau pure est de 6,14, ce qui est encore neutre sur l’échelle du pH même s’il est inférieur à 7.
Aussi, comment calcule-t-on le pH de l’eau pure ?
Le pH de l’eau pure est de 7, soit le logarithme négatif de 1 X 10–7. Une solution neutre est une solution qui n’est ni acide ni basique. La concentration en ions hydrogène est égale à la concentration en ions hydroxyde, et les deux sont égales à 1 X 10–7 M. Dans une solution neutre, alors, pH = pOH = 7.
À cet égard, quel est le pH de l’eau pure à 37 degrés Celsius ?
À 37 ° C le logK est égal à -13,63 donc le pH est de 6,815. Avec l’augmentation de la température, la différence entre les deux fonctions s’accroît.
Quel est le pH de 100 ml d’eau pure à 25 ?
L’eau pure toute seule est toujours neutre pH , ni acide ni basique, par définition. Les molécules d’eau doivent toujours s’ioniser en H+ et OH- en quantités égales. Les concentrations en ions H+ et OH- seront les mêmes. Le » pH neutre » de l’ eau est de 7,0 à environ 25 deg C ou environ 77 deg F.
Quels sont les facteurs qui affectent le pH ?
Quels facteurs peuvent affecter le pH de l’eau potable ?
- Concentration de dioxyde de carbone dans l’eau. Malheureusement, en raison du réchauffement climatique, les émissions de dioxyde de carbone dans notre atmosphère ont augmenté au fil des ans.
- Les pluies acides.
- Les minéraux dissous.
- La température.
- Les eaux usées.
L’eau bouillante augmente-t-elle le pH ?
Le pH diminue très légèrement lorsqu’on fait bouillir l’ eau , car le taux d’ionisation directe augmente . Cependant, cela ne signifie pas que l’ eau est maintenant acide, mais plutôt que le point neutre est maintenant légèrement inférieur à 7. Cela signifie qu’à cette température plus élevée, le pH neutre n’est pas 7 mais plutôt 6.
La pression affecte-t-elle le pH ?
Selon la loi de Henry, la quantité de gaz dissous est proportionnelle à sa pression partielle . Ainsi, si l’on considère le cas où la pression atmosphérique augmente, davantage de dioxyde de carbone se dissoudra dans la solution, diminuant son pH .
Qu’est-ce qui provoque un faible pH dans l’eau ?
Le dioxyde de carbone est la cause la plus courante de l’acidité de l’ eau ¹5. La photosynthèse, la respiration et la décomposition contribuent toutes aux fluctuations du pH en raison de leurs influences sur les niveaux de CO2. Cela augmente le H2CO3, qui diminue le pH . Cet effet devient plus évident dans les études sur le pH océanique au fil du temps.
Le pH affecte-t-il la température ?
* pH diminue avec l’augmentation de la température . Mais cela ne signifie pas que l’eau devient plus acide à des températures plus élevées. Une solution est considérée comme acide s’il y a un excès d’ions hydrogène par rapport aux ions hydroxyde. A 100°C, une valeur pH de 6,14 est le nouveau point neutre sur l’échelle pH à cette température plus élevée.
Le pH peut-il être négatif ?
Il est tout à fait possible de calculer une valeur de pH négative. En pratique, tout acide qui donne une concentration d’ions hydrogène avec une molarité supérieure à 1 sera calculé pour avoir un pH négatif . Par exemple, le pH de 12M HCl (acide chlorhydrique) est calculé pour être -log(12) = -1,08.
Comment KW affecte-t-il le pH ?
Pour trouver le pH , vous devez d’abord trouver la concentration en ions hydrogène (ou en ions hydroxonium – c’est la même chose). Ensuite, vous la convertissez en pH . Mais dans l’eau pure, la concentration en ions hydrogène (ions hydroxonium) doit être égale à la concentration en ions hydroxyde.
| T (°C) | Kw (mol2 dm–6) | pH |
|---|---|---|
| 100 | 51,3 x 10–14 | 6,14 |
Qu’est-ce qu’un pH normal ?
Le pH sanguin : l’acidité ou l’alcalinité du sang. Le pH de tout fluide est la mesure de la concentration en ions hydrogène (H–). Un pH de 7 est neutre. Plus le pH est bas, plus le sang est acide. Le pH sanguin normal est étroitement régulé entre 7,35 et 7,45.
Quel est le pH du lait ?
6,5 à 6,7
Comment trouve-t-on le pH ?
Pour calculer le pH d’une solution aqueuse, il faut connaître la concentration de l’ion hydronium en moles par litre (molarité). Le pH est alors calculé à l’aide de l’expression : pH = – log [H3O+].
Quel est le pH de l’eau distillée ?
L’eau pure distillée devrait être neutre avec un pH de 7, mais comme elle absorbe le dioxyde de carbone de l’atmosphère, elle est en fait légèrement acide avec un pH de 5,8.
Pourquoi le pH augmente-t-il avec la température ?
Le pH à la température ambiante est de ~7, ce qui signifie qu’il y a environ 10-7 moles de H+ par litre d’eau à la température ambiante. Lorsque la température augmente , la capacité de l’eau à s’ioniser de cette manière augmente et donc la concentration de H+ en solution va augmenter (et donc le pH va baisser).
Quel est le pH du vinaigre ?
Mesurer la valeur pH du vinaigre
Le vinaigre blanc distillé mesure généralement autour de pH 2,4, avec une force de 5%. Plus le pH est bas, plus le vinaigre est acide. Si vous utilisez le vinaigre comme liquide de démarrage pour la fabrication du kombucha, il devrait avoir un pH ne dépassant pas 4,5, et une force d’au moins 5%.
Quel est le pH de la peau ?
La valeur optimale du pH de la peau de la plupart de notre visage et de notre corps se situe entre 4,7 et 5,75. Un pH de 7 (celui de l’eau pure) est considéré comme neutre. Tout ce qui est en dessous est acide et au-dessus alcalin, donc le pH naturel de la peau est légèrement acide.
L’eau bouillie est-elle alcaline ou acide ?
L’eau dérivée des filtres à eau domestiques avait un pH approximatif de 7,5 identique à celui de l’ eau du robinet , alors que l’ eau bouillie du robinet avait un pH alcalin légèrement supérieur.
Que signifie pH ?
hydrogène potentiel
Pourquoi le pH de l’eau est-il de 7 ?
pH est une mesure de la quantité d’ions hydrogène (H+) dans une solution. Même dans l’ eau pure, les ions ont tendance à se former en raison de processus aléatoires (produisant quelques ions H+ et OH-). La quantité de H+ qui est fabriquée dans l’ eau pure est à peu près égale à un pH de 7 . C’est pourquoi 7 est neutre.
Concentration de dioxyde de carbone dans l\'eau. Malheureusement, en raison du réchauffement climatique, les émissions de dioxyde de carbone dans notre atmosphère ont augmenté au fil des ans. Les pluies acides. Les minéraux dissous. La température. Les eaux usées. " } }, {"@type": "Question","name": " L\'eau bouillante augmente-t-elle le pH ? ","acceptedAnswer": {"@type": "Answer","text": " Le pH diminue très légèrement lorsqu\'on fait bouillir l\'eau, car le taux d\'ionisation directe augmente. Cependant, cela ne signifie pas que l\'eau est maintenant acide, mais plutôt que le point neutre est maintenant légèrement inférieur à 7. Cela signifie qu\'à cette température plus élevée, le pH neutre n\'est pas 7 mais plutôt 6." } }, {"@type": "Question","name": " La pression affecte-t-elle le pH ? ","acceptedAnswer": {"@type": "Answer","text": " Selon la loi de Henry, la quantité de gaz dissous est proportionnelle à sa pression partielle. Ainsi, si l\'on considère le cas où la pression atmosphérique augmente, davantage de dioxyde de carbone se dissoudra dans la solution, diminuant son pH." } }, {"@type": "Question","name": " Qu\'est-ce qui provoque un faible pH dans l\'eau ? ","acceptedAnswer": {"@type": "Answer","text": " Le dioxyde de carbone est la cause la plus courante de l\'acidité de l\'eau ¹5. La photosynthèse, la respiration et la décomposition contribuent toutes aux fluctuations du pH en raison de leurs influences sur les niveaux de CO2. Cela augmente le H2CO3, qui diminue le pH. Cet effet devient plus évident dans les études sur le pH océanique au fil du temps." } }, {"@type": "Question","name": " Le pH affecte-t-il la température ? ","acceptedAnswer": {"@type": "Answer","text": " *pH diminue avec l\'augmentation de la température. Mais cela ne signifie pas que l\'eau devient plus acide à des températures plus élevées. Une solution est considérée comme acide s\'il y a un excès d\'ions hydrogène par rapport aux ions hydroxyde. A 100°C, une valeur pH de 6,14 est le nouveau point neutre sur l\'échelle pH à cette température plus élevée." } }, {"@type": "Question","name": " Le pH peut-il être négatif ? ","acceptedAnswer": {"@type": "Answer","text": " Il est tout à fait possible de calculer une valeur de pH négative. En pratique, tout acide qui donne une concentration d\'ions hydrogène avec une molarité supérieure à 1 sera calculé pour avoir un pH négatif. Par exemple, le pH de 12M HCl (acide chlorhydrique) est calculé pour être -log(12) = -1,08." } }, {"@type": "Question","name": " Qu\'est-ce qu\'un pH normal ? ","acceptedAnswer": {"@type": "Answer","text": " Le pH sanguin : l\'acidité ou l\'alcalinité du sang. Le pH de tout fluide est la mesure de la concentration en ions hydrogène (H-). Un pH de 7 est neutre. Plus le pH est bas, plus le sang est acide. Le pH sanguin normal est étroitement régulé entre 7,35 et 7,45.
" } }, {"@type": "Question","name": "Comment trouve-t-on le pH ? ","acceptedAnswer": {"@type": "Answer","text": " Pour calculer le pH d\'une solution aqueuse, il faut connaître la concentration de l\'ion hydronium en moles par litre (molarité). Le pH est alors calculé à l\'aide de l\'expression : pH = - log [H3O+]." } }, {"@type": "Question","name": " Quel est le pH de l\'eau distillée ? ","acceptedAnswer": {"@type": "Answer","text": " L\'eau pure distillée devrait être neutre avec un pH de 7, mais comme elle absorbe le dioxyde de carbone de l\'atmosphère, elle est en fait légèrement acide avec un pH de 5,8." } }, {"@type": "Question","name": " Pourquoi le pH augmente-t-il avec la température ? ","acceptedAnswer": {"@type": "Answer","text": " Le pH à la température ambiante est de ~7, ce qui signifie qu\'il y a environ 10-7 moles de H+ par litre d\'eau à la température ambiante. Lorsque la température augmente, la capacité de l\'eau à s\'ioniser de cette manière augmente et donc la concentration de H+ en solution va augmenter (et donc le pH va baisser)." } }, {"@type": "Question","name": " Quel est le pH du vinaigre ? ","acceptedAnswer": {"@type": "Answer","text": "Mesurer la valeur pH du vinaigre
Le vinaigre blanc distillé mesure généralement autour de pH 2,4, avec une force de 5%. Plus le pH est bas, plus le vinaigre est acide. Si vous utilisez le vinaigre comme liquide de démarrage pour la fabrication du kombucha, il devrait avoir un pH ne dépassant pas 4,5, et une force d\'au moins 5%." } }, {"@type": "Question","name": " Quel est le pH de la peau ? ","acceptedAnswer": {"@type": "Answer","text": " La valeur optimale du pH de la peau de la plupart de notre visage et de notre corps se situe entre 4,7 et 5,75. Un pH de 7 (celui de l\'eau pure) est considéré comme neutre. Tout ce qui est en dessous est acide et au-dessus alcalin, donc le pH naturel de la peau est légèrement acide." } }, {"@type": "Question","name": " L\'eau bouillie est-elle alcaline ou acide ? ","acceptedAnswer": {"@type": "Answer","text": " L\'eau dérivée des filtres à eau domestiques avait un pH approximatif de 7,5 identique à celui de l\'eau du robinet, alors que l\'eau bouillie du robinet avait un pH alcalin légèrement supérieur." } }] }