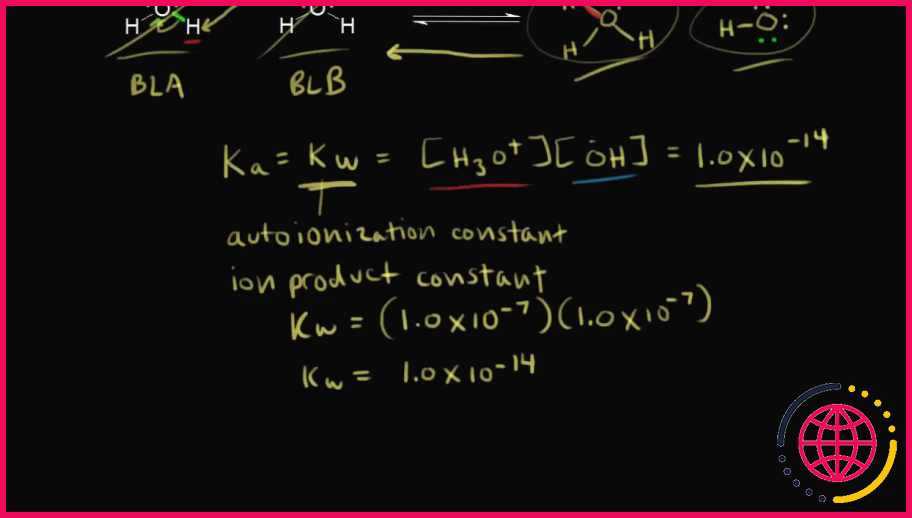Quelle est la concentration de h+ et de oh dans l’eau pure ?
Une solution neutre est une solution qui n’est ni acide ni basique. L’ion hydrogène concentration est égal à l’ion hydroxyde concentration , et les deux sont égaux à 1 X 10–7 M. Dans une solution neutre, alors, pH = pOH = 7.
L’eau comme acide faible.
| [H+][ OH –] = | (x)(x) = 1 X 10–14 |
|---|---|
| x = | 1 X 10–7 |
| [H+] = | [ OH –] = 1 X 10–7 M |
En tenant compte de cela, quelle est la concentration de OH dans l’eau pure ?
Dans l’eau pure , à 25C, les [H3O+]et [ OH –]concentrations des ions sont de 1,0 x 10–7 M. La valeur de Kw à 25C est donc de 1,0 x 10–14. Bien que Kw soit défini en termes de dissociation de l’ eau , cette expression de la constante d’équilibre est également valable pour les solutions d’acides et de bases dissoutes dans l’ eau .
Deuxièmement, que pouvons-nous dire de la concentration de H+ par rapport à la concentration de OH dans l’eau ?
Plus la concentration de H3O+ (ou H+) dans une solution est élevée, plus la solution est acide. Plus la concentration de OH – dans une solution est élevée, plus la solution est basique. L’ eau pure subit une réaction réversible dans laquelle sont générés à la fois H+ et OH –.
Donc, qu’est-ce que cela signifie en termes de concentration de OH et H+ ?
Cela indique la concentration des ions hydrogène (H+) et des ions hydroxyde ( OH -) dans une solution. Ces concentrations d’ions sont égales dans l’eau pure, dont le pH est de 7.
Qu’est-ce que H+ dans l’eau pure ?
Dans l’ eau pure , la concentration en ions hydrogène, [H+], est égale à la concentration en ions hydroxyde, [OH–]. Le pH de l’ eau pure est de 7, soit le logarithme négatif de 1 X 10–7. Une solution neutre est une solution qui n’est ni acide ni basique. La concentration en ions hydrogène est égale à la concentration en ions hydroxyde, et les deux sont égales à 1 X 10–7 M.
Que trouve-t-on dans l’eau pure ?
L’eau , H2O, est une substance pure , un composé constitué d’hydrogène et d’oxygène. Bien que l’ eau soit la substance la plus abondante sur terre, on la trouve rarement à l’état naturel sous sa forme pure . La plupart du temps, l’ eau pure doit être créée. L’eau pure est appelée eau distillée ou eau déionisée .
Comment la concentration en H+ affecte-t-elle le pH ?
Plus la concentration en H+ est élevée, plus le pH est faible, et plus la concentration en OH- est élevée, plus le pH est élevé. A un pH neutre de 7 (eau pure), la concentration des ions H+ et des ions OH- est de 10?7 M. En raison de cette influence, H+ et OH- sont liés aux définitions de base des acides et des bases.
Quelle est la formule pour calculer le pH ?
Vous pouvez calculer le pH d’une solution acide ou basique étant donné la concentration de l’ion hydronium en utilisant la formule pH = -log [ H3O+] ou si étant donné la concentration de l’ion hydroxyde par la formule [ H3O+] = Kw / [OH-], alors en utilisant la formule pH = -log [ H3O+] .
Quel est le pH de l’eau ?
6,5 à 8,5
Comment trouver la concentration en OH ?
Trouvez le [ OH –] étant donné le pH ou le pOH. On vous donne que le pH = 4,5. Trouvez la concentration en ions hydroxyde d’une solution dont le pOH est de 5,90. Pour résoudre cette question, utilisez une calculatrice scientifique et entrez 5,90 et utilisez le bouton +/- pour le rendre négatif, puis appuyez sur la touche 10x.
Quel est le pKa de l’eau pure à 25 C ?
Le pKa de l’ eau à 25 ° C est de 14,0 et non de 15,7(4) comme couramment cité.
Quelle est la concentration de H+ dans l’eau ?
L’eau se décompose en ses ions, H2O <==> ; H+ + OH-, dans une mesure très, très limitée, mais suffisante pour qu’il y ait des ions hydrogène dans l’ eau . Si une solution est acide, sa concentration d’ions hydrogène [H+] est supérieure à 1 x 10^-7. Si elle est basique, sa concentration en ions hydrogène est inférieure à 1 x 10^-7.
H+ est-il acide ou basique ?
Si l’un de ces ions est H+, la solution est acide. L’acide fort hydrogène chlorure (HCl) en est un exemple. Si l’un de ces ions est OH–, la solution est basique. Un exemple de base forte est l’hydroxyde de sodium (NaOH).
Qu’est-ce que la concentration de H+ ?
Dans une eau acide, il y a une augmentation de la concentration d’atomes d’hydrogène chargés positivement, H+ . Cette concentration détermine la valeur du pH. Entrez dans la calculatrice la valeur de pH pour laquelle vous avez l’intention de calculer la concentration de H+ . Par exemple, si le pH de votre solution est de 5, entrez 5 dans la calculatrice.
Le NaOH est-il un acide ou une base ?
NaOH est une base car lorsqu’il est dissous dans l’eau, il se dissocie en ions Na+ et OH-. C’est le OH- (ion hydroxyle) qui fait du NaOH une base . En termes classiques, une base est définie comme un composé qui réagit avec un acide pour former du sel et de l’eau, comme représenté par l’équation suivante.
H+ est-il égal à Oh ?
Une solution neutre aura des ions H+ égaux aux ions OH -. Une substance neutre aura un pH de 7. > ; Un exemple de solution neutre est l’eau : le # d’ions H+ = le # d’ions OH -. > ; Si l’eau est combinée avec plus d’ions H+ , elle deviendra plus acide. >
Quel type de réaction est H+ OH h2o ?
Quel type de réaction l’équation représente-t-elle ? Par définition, la neutralisation se produit lorsque des quantités égales d’un acide (H+) réagissent avec des quantités égales d’une base (OH-) pour former de l’ eau .
Comment H+ et OH sont-ils liés ?
Comme le pH et le pOH, il existe également une relation entre l’ion [ H+ ] et l’ion [ OH -]. Plus il y a d’ions [ H+ ] en solution, plus la solution est acide. Plus il y a d’ions [ OH -] en solution, plus la solution est basique.
Qu’est-ce qu’un acide par rapport à une base ?
Les acides sont définis comme des composés qui donnent un ion hydrogène (H+) à un autre composé (appelé une base ). Corrélativement, une base était tout composé qui, lorsqu’il est dissous dans l’eau, donne une solution dont l’activité en ions hydrogène est inférieure à celle de l’eau pure, c’est-à-dire un pH supérieur à 7,0 dans les conditions normales.
Qu’est-ce qui rend une solution neutre ?
Par définition, une solution neutre est une solution qui a un pH de 7. Elle n’est ni acide (pH < ; 7) ni basique (pH > ; 7), mais juste au milieu, ou neutre .
Qu’est-ce qui rend l’eau pure neutre ?
Le pH étant défini comme le log négatif de la concentration en ions hydrogène, le pH de l’ eau pure est de 7 ou neutre . L’eau pure est neutre car le nombre d’ions hydrogène positifs produits est égal au nombre d’ions négatifs.
Quelle est la concentration de H+ dans l’eau pure à 25 C ?
Au 25 ° C , l’ eau pure devrait contenir 1E-7 moles de H+ par dm3 d’ eau . Lorsque la température de l’ eau pure est élevée, le principe de Le Chatiler stipule qu’elle favorisera la réaction endothermique, entraînant une concentration plus élevée de H+ . Bien entendu, la concentration de OH- augmente également dans le même rapport.