Quels types d’alcools peuvent être oxydés ?
Les alcools primaires (R-CH2-OH) peuvent être oxydés soit en aldéhydes (R-CHO) soit en acides carboxyliques (R-CO2H), tandis que l’oxydation des alcools secondaires (R1R2CH-OH) se termine normalement au stade de la cétone (R1R2C=O). Les alcools tertiaires (R1R2R3C-OH) sont résistants à l’oxydation.
A cet égard, tous les alcools peuvent-ils être oxydés ?
L’ oxydation des alcools est une réaction importante en chimie organique. Les alcools primaires peuvent être oxydés pour former des aldéhydes et des acides carboxyliques ; les alcools secondaires peuvent être oxydés pour donner des cétones. Les alcools tertiaires, en revanche, ne peuvent pas être oxydés sans rompre les liaisons C-C de la molécule.
On peut aussi se demander si les alcools tertiaires peuvent être oxydés. Les alcools tertiaires ne sont pas oxydés par une solution acidifiée de dichromate(VI) de sodium ou de potassium. Il n’y a pas la moindre réaction. Les alcools tertiaires n’ont pas d’atome d’hydrogène attaché à ce carbone.
Par la suite, on peut aussi se demander quel type d’alcool est le plus facilement oxydé ?
2. Test d’oxydation
- L’alcool primaire s’oxyde facilement en aldéhyde et peut aussi s’oxyder en acide carboxylique.
- L’alcool secondaire s’oxyde facilement en cétone mais l’oxydation ultérieure n’est pas possible.
- L’alcool tertiaire ne s’oxyde pas en présence de dichromate de sodium.
Que se passe-t-il lorsque les alcools sont oxydés ?
Les alcools primaires peuvent être oxydés en aldéhydes ou en acides carboxyliques, selon les conditions de réaction. Dans le cas de la formation d’acides carboxyliques, l’ alcool est d’abord oxydé en un aldéhyde, qui est ensuite oxydé de nouveau en acide.
Pourquoi l’oxydation des alcools est-elle importante ?
Oxydation des alcools en aldéhydes ou cétones : Importance biologique. La oxydation des groupes alcool en groupes carbonyles représente une étape importante dans la dégradation des graisses au cours du métabolisme humain (par exemple, L- malate en oxaloacétate). De telles oxydations font également partie du cycle de l’acide citrique.
L’alcool est-il un oxydant ?
L’oxydation de l’alcool est une réaction organique importante. Les alcools primaires (R-CH2-OH) peuvent être oxydés soit en aldéhydes (R-CHO) soit en acides carboxyliques (R-CO2H), tandis que l’oxydation des alcools secondaires (R1R2CH-OH) se termine normalement au stade de la cétone (R1R2C=O).
Où l’alcool est-il oxydé dans l’organisme ?
Le foie est le principal site d’ oxidation de l’ alcool , une partie de l’ alcool est oxydée le dans l’estomac, également. Le métabolite primaire de l’oxydation de l’éthanol est l’acétaldéhyde.
Comment distinguer les alcools primaires des alcools secondaires ?
Comment pourrait-on distinguer entre un alcool primaire et secondaire ? Réchauffez et distillez avec du bichromate de pottasium acidifié. Puis testez avec le réactif de Tollens. Le bichromate de pottasium acidifié aura oxydé l’alcool primaire en un aldéhyde, qui formera un miroir d’argent avec le réactif de Tollen.
Comment se forment les alcools ?
Les alcools peuvent être formés en utilisant la fermentation. La fermentation se fait généralement en utilisant des levures qui agissent sur les glucides pour produire de l’éthanol et du dioxyde de carbone. Le riz, le malt, les fruits et autres, qui sont des sources de glucides, sont utilisés pour réagir avec la levure. Les alcools peuvent être formés en faisant réagir des alcènes avec l’eau .
Les alcools primaires ou secondaires s’oxydent-ils plus vite ?
Pourquoi les alcools primaires s’oxydent-ils plus vite que les secondaires ? Parce que les alcools secondaires ont un plus grand effet stérique dû au carbone supplémentaire ce qui signifie qu’il réagira plus lentement que l’alcool primaire .
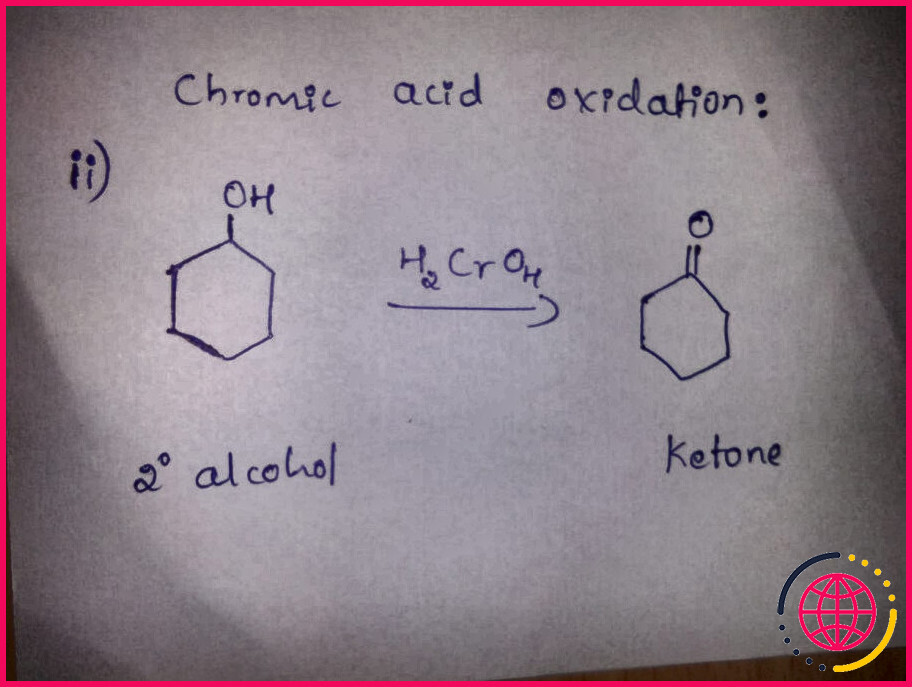
Comment oxyde-t-on un alcool secondaire ?
Oxydation des alcools secondaires en cétones. L’ oxidation des alcools secondaires en cétones est une réaction importante d’ oxidation en chimie organique. Lorsqu’un alcool secondaire est oxydé , il est converti en cétone. L’hydrogène du groupe hydroxyle est perdu ainsi que l’hydrogène lié au deuxième carbone.
Avec quoi réagissent les alcools ?
Les alcools peuvent être oxydés pour donner des aldéhydes, des cétones et des acides carboxyliques. L’oxydation des composés organiques augmente généralement le nombre de liaisons du carbone à l’oxygène, et elle peut diminuer le nombre de liaisons à l’hydrogène. Les alcools tertiaires ne réagissent pas avec . de l’acide chromique dans des conditions douces.
Quel est le métal le plus facilement oxydé ?
Quel métal est le plus facilement oxydé ? Parmi les métaux que l’on peut pratiquement collecter et manipuler, le césium est le plus facilement oxydable . Exposé à l’oxygène de l’air, il prend feu.
Le kmno4 peut-il oxyder un alcool tertiaire ?
Oui, c’est exact. Les alcools tertiaires subissent facilement une élimination pour donner des alcènes, puis le KMNO4 réagit avec l’alcène pour donner une dihydroxylation syn.
Qu’est-ce que l’oxydation de l’éthanol ?
Lorsque l’ éthanol est oxydé , il gagne un atome d’oxygène et deux liaisons carbone-oxygène supplémentaires. Le produit d’une réaction d’ oxydation de l’éthanol est un composé appelé acide acétique, qui contient un groupe fonctionnel acide carboxylique.
Comment l’alcool est-il transformé en ester ?
Pour fabriquer un petit ester comme l’éthanoate d’éthyle, on peut chauffer doucement un mélange d’acide éthanoïque et d’ éthanol en présence d’acide sulfurique concentré, et distiller le ester dès qu’il est formé. Cela évite que la réaction inverse ne se produise.
Pourquoi les alcools primaires sont-ils plus réactifs ?
Les alcools tertiaires sont plus réactifs parce que l’augmentation du nombre de groupes alkyle augmente l’effet +I. Donc, la densité de charge sur l’atome de carbone augmente et donc autour de l’atome d’oxygène. Par conséquent, le clivage de la liaison C-O devient plus facile. Ainsi, un carbocation tertiaire est formé qui est plus stable que le secondaire et le primaire .
Comment peut-on réduire l’alcool ?
Les alcools primaires peuvent être désoxygénés proprement et avec de bons rendements par réduction des esters de phosphate de diphényle dérivés avec le triéthylborohydrure de lithium dans le THF à température ambiante. Les alcools primaires peuvent être sélectivement réduits en présence d’ alcools secondaires.
L’alcool est-il alcalin ou acide ?
Avec un pKa d’environ 16-19, ils sont, en général, des acides légèrement plus faibles que l’eau. Avec des bases fortes comme l’hydrure de sodium ou le sodium, ils forment des sels appelés alcoxydes, de formule générale RO– M+. L’acidité des alcools est fortement influencée par la solvatation. En phase gazeuse, les alcools sont plus acides que dans l’eau.
Comment l’alcool est-il transformé en alcène ?
Déshydratation des alcools pour générer des alcènes La réaction de déshydratation des alcools pour générer des alcènes se déroule en chauffant les alcools en présence d’un acide fort, comme l’acide sulfurique ou phosphorique, à haute température.
Pourquoi les alcools tertiaires ne sont-ils pas oxydés ?
Les alcools tertiaires (R 3COH) sont résistants à l’ oxydation car l’atome de carbone qui porte le groupe OH n’a pas d’atome d’hydrogène attaché mais est au contraire lié à d’autres atomes de carbone. Par conséquent, les alcools tertiaires ne sont pas facilement oxydés .