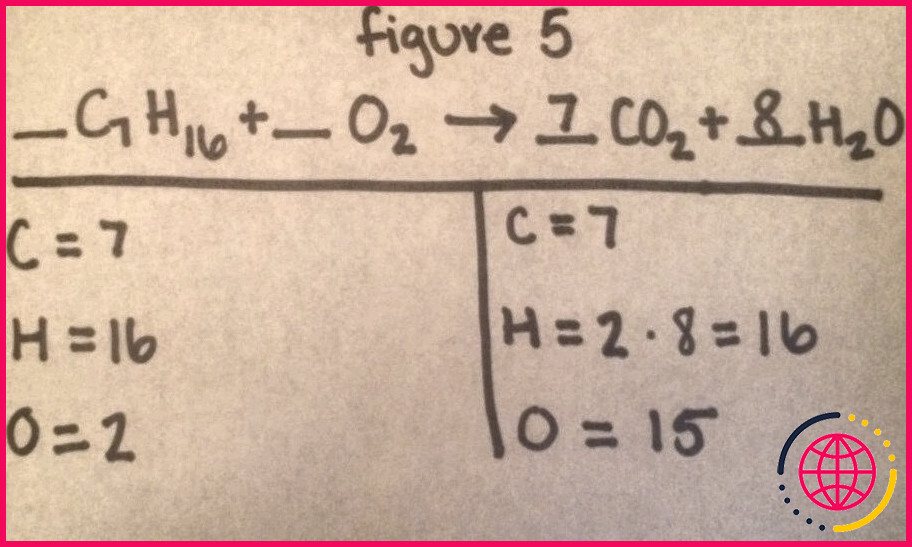Qu’est-ce que l’équilibrage d’une équation chimique ?
L’ équation chimique doit être équilibrée pour qu’elle respecte la loi de conservation de la masse. Une équation chimique équilibrée se produit lorsque le nombre des différents atomes d’éléments du côté des réactifs est égal à celui du côté des produits. L’équilibrage des équations chimiques est un processus d’essais et d’erreurs.
En tenant compte de cela, comment équilibrer une équation chimique ?
Pour équilibrer une équation chimique , commencez par écrire le nombre d’atomes de chaque élément, qui est répertorié dans l’indice à côté de chaque atome. Ensuite, ajoutez des coefficients aux atomes de chaque côté de l’ équation pour les équilibrer avec les mêmes atomes de l’autre côté.
En outre, quelles sont les règles pour équilibrer les équations chimiques ?
Conseil : commencez par équilibrer un élément qui apparaît dans un seul réactif et un seul produit. Une fois qu’un élément est équilibré, procédez à l’équilibrage d’un autre, et d’un autre, jusqu’à ce que tous les éléments soient équilibrés. Equilibrez les formules chimiques en plaçant des coefficients devant elles. N’ajoutez pas d’indices, car cela modifierait les formules.
À part cela, quel est le but d’équilibrer une équation chimique ?
La raison pour équilibrer des équations en chimie est d’obtenir les bonnes proportions de réactifs et de produits pour une réaction donnée. Comme les réactions chimiques ne changent pas les atomes eux-mêmes, une équation équilibrée vous indique la quantité de produit à attendre pour un ensemble donné de réactifs.
Quels sont les types de réactions chimiques ?
Les quatre principaux types de réactions sont la combinaison directe, la réaction d’analyse, le déplacement simple et le déplacement double. Si on vous demande les cinq principaux types de réactions , ce sont ces quatre-là et ensuite soit acide-base, soit oxydoréduction (selon qui vous demandez).
Quels sont les exemples d’équation chimique ?
Formule de réaction chimique Exemples : 1. Le méthane (CH4) et l’oxygène (O2) réagissent pour produire du dioxyde de carbone (CO2) et de l’eau (H2O). CH4 et O2 sont les réactifs, tandis que CO2 et H2O sont les produits.
Que signifie catalyseur ?
Un catalyseur est une substance qui accélère une réaction chimique, mais qui n’est pas consommée par la réaction ; par conséquent, un catalyseur peut être récupéré chimiquement inchangé à la fin de la réaction qu’il a été utilisé pour accélérer, ou catalyser.
Quelle est l’équation de la réaction chimique ?
Équation chimique. Une équation chimique est la représentation symbolique d’une réaction chimique sous forme de symboles et de formules, dans laquelle les entités du réactif sont données du côté gauche et les entités du produit du côté droit.
Comment la loi de conservation de la matière s’applique-t-elle aux réactions chimiques ?
La matière ne peut pas être créée ou détruite dans les réactions chimiques . C’est la loi de conservation de la masse. Dans chaque réaction chimique , la même masse de matière doit se retrouver dans les produits que celle qui a commencé dans les réactifs. Les équations chimiques équilibrées montrent que la masse se conserve dans les réactions chimiques .
Combien de types d’équations chimiques existe-t-il ?
cinq
Quelles sont les deux raisons pour lesquelles il faut équilibrer les équations chimiques ?
Les équations chimiques sont équilibrées afin de : 1) satisfaire la Loi de Conservation de la masse, et 2) établir les relations molaires nécessaires aux calculs stœchiométriques. La Loi de la Conservation de la masse : La Loi de Conservation de la masse stipule que la masse ne peut être créée ou détruite.
Quelle est la définition de l’énergie d’activation en chimie ?
Le terme Énergie d’activation a été introduit en 1889 par Svante Arrhenius, un scientifique suédois. Elle est définie comme étant la plus petite quantité possible d’ énergie (minimum) qui est nécessaire pour démarrer une réaction ou la quantité d’ énergie disponible dans un système chimique pour qu’une réaction ait lieu.
Quels sont les 4 types de réactions chimiques ?
Représentation des quatre types de réactions chimiques de base : synthèse, décomposition , remplacement simple et double remplacement.