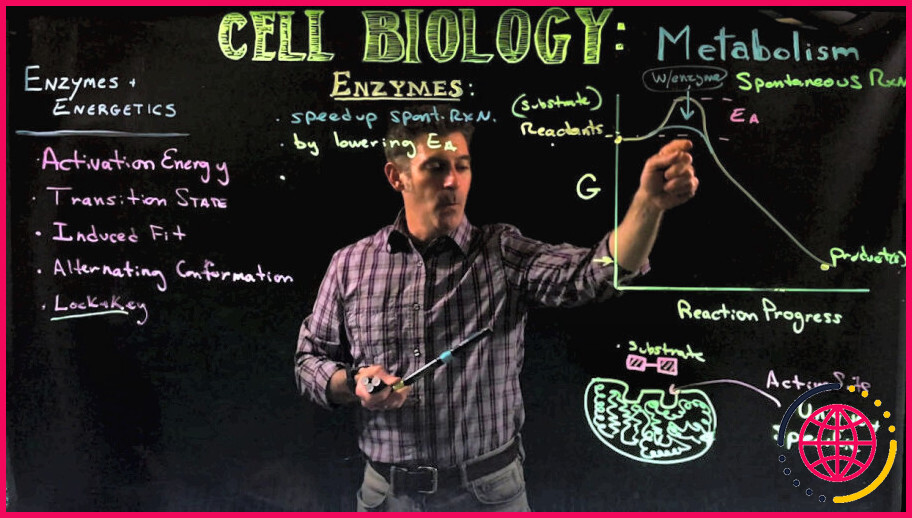
Comment une enzyme abaisse-t-elle l’énergie d’activation d’une réaction ?
Les enzymes abaissent l’ énergie d’activation d’une réaction en liant l’un des réactifs, appelé substrat, et en le maintenant d’une manière qui abaisse l’ énergie d’activation .
De même, vous pouvez vous demander comment les enzymes affectent l’énergie d’activation ?
Les enzymes sont des catalyseurs, donc elles affectent l’énergie d’activation en diminuant la quantité requise d’énergie d’activation permettant aux réactions chimiques de se produire ou de s’accélérer. Ils ne affectent pas la quantité d’ énergie qui est libérée par la réaction.
Par ailleurs, comment le site actif diminue-t-il l’énergie d’activation ? Le site actif est constitué de résidus qui forment des liaisons temporaires avec le substrat ( site de liaison ) et de résidus qui catalysent une réaction de ce substrat ( site catalytique ). Ce processus est réalisé en abaissant l’ énergie d’activation de la réaction, de sorte que davantage de substrats ont suffisamment d’ énergie pour subir la réaction.
En gardant cela à l’esprit, comment les enzymes abaissent-elles l’énergie d’activation d’une réaction quizlet ?
Les enzymes abaissent l’énergie d’activation par divers moyens, notamment en positionnant les substrats ensemble dans la bonne orientation, en appliquant un couple sur les substrats, en fournissant la charge appropriée ou le microenvironnement de pH, et en ajoutant ou en retirant des groupes fonctionnels sur les substrats.
Pourquoi une énergie d’activation plus faible augmente-t-elle la vitesse de réaction ?
Vitesses de réaction Un catalyseur augmente l’ énergie des molécules réactives afin qu’une réaction chimique puisse avoir lieu. Un catalyseur abaisse l’ énergie d’activation d’une réaction , de sorte qu’une réaction chimique peut avoir lieu.
Que se passe-t-il lorsque l’énergie d’activation est diminuée ?
La énergie nécessaire au démarrage d’une réaction est appelée énergie d’activation . Plus la baisse de l’énergie d’activation est importante, plus une réaction se produit rapidement. Les réactifs ont une énergie plus élevée que les produits. La énergie des réactifs augmente puis diminue jusqu’à la énergie du produit final.
Pourquoi l’énergie d’activation est-elle importante ?
Toutes les réactions chimiques, y compris les réactions exothermiques, ont besoin d’une énergie d’activation pour démarrer. L’énergie d’activation est nécessaire pour que les réactifs puissent se rapprocher, surmonter les forces de répulsion et commencer à rompre les liaisons.
Quel est un exemple de l’utilisation de l’énergie d’activation ?
Cette énergie est appelée énergie d’activation . Pour exemple , l’ énergie d’activation est nécessaire pour démarrer le moteur d’une voiture. Tourner la clé provoque une étincelle qui active la combustion de l’essence dans le moteur. La combustion de l’essence ne se produira pas sans l’étincelle de énergie pour amorcer la réaction.
Comment trouver l’énergie d’activation ?
La valeur de la pente (m) est égale à -Ea/R où R est une constante égale à 8,314 J/mol-K. L’ énergie d’activation peut également être trouvée algébriquement en substituant deux constantes de vitesse (k1, k2) et les deux températures de réaction correspondantes (T1, T2) dans l’équation d’Arrhenius (2).
Quelle est l’énergie d’activation d’une réaction ?
L’ énergie d’activation de la réaction directe est la quantité d’ énergie libre qui doit être ajoutée pour passer du niveau d’ énergie des réactifs au niveau d’ énergie de l’état de transition.
Comment les enzymes sont-elles activées ?
Les enzymes sont des protéines qui catalysent les réactions dans les cellules. Certaines enzymes doivent être activées pour pouvoir fonctionner. Les activateurs sont des effecteurs qui se lient à un site allostérique et aident le substrat à se fixer. Les cofacteurs peuvent également être nécessaires pour activer une enzyme ; ils aident le substrat à s’insérer dans le site actif.
Qu’est-ce qui affecte l’activité enzymatique ?
Plusieurs facteurs affectent la vitesse à laquelle se déroulent les réactions enzymatiques – la température, le pH, la concentration en enzyme , la concentration en substrat, et la présence de tout inhibiteur ou activateur.
Que signifie l’énergie d’activation d’une réaction ?
Le terme énergie d’activation a été introduit en 1889 par Svante Arrhenius, un scientifique suédois. Elle est définie comme la plus petite quantité possible d’ énergie (minimum) qui est nécessaire pour démarrer une réaction ou la quantité d’ énergie disponible dans un système chimique pour qu’une réaction ait lieu.
Quelles sont les molécules qui abaissent l’énergie d’activation des réactions biochimiques ?
Les enzymes sont de grandes protéines qui lient de petites molécules. Lorsqu’elles sont liées à une enzyme .
En effet, les liaisons des réactifs peuvent être tendues (c’est-à-dire étirées), ce qui leur permet d’atteindre plus facilement l’état de transition. C’est l’une des façons dont les enzymes réduisent l’énergie d’activation d’une réaction.
L’ajout d’une enzyme réduit-il l’énergie d’activation requise pour une réaction ?
Une substance qui aide une réaction chimique à se produire est appelée un catalyseur, et les molécules qui catalysent les réactions biochimiques sont appelées enzymes . Elles ne font que réduire l’énergie d’activation requise pour que la réaction se déroule (figure 1). En addition , une enzyme elle-même est inchangée par la réaction qu’elle catalyse.
Quelle est la principale façon dont les enzymes abaissent l’énergie d’activation ?
Par rapport à une réaction non catalysée (à gauche), les enzymes abaissent l’énergie d’activation en stabilisant l’état de transition dans une conformation plus favorable sur le plan énergétique (à droite). Les Enzymes facilitent les réactions chimiques en abaissant l’ énergie d’activation nécessaire pour que la réaction se produise.
En quoi les ribozymes sont-ils différents des enzymes ?
Un ribozyme est un acide ribonucléique (ARN) enzyme qui catalyse une réaction chimique. Le ribozyme catalyse des réactions spécifiques de manière similaire à celle des enzymes protéiques. Également appelés ARN catalytiques, les ribozymes se trouvent dans le ribosome où ils unissent les acides aminés pour former des chaînes de protéines.
Pourquoi votre corps a-t-il besoin de tant d’enzymes différentes ?
Réponse et explication : Le corps humain a besoin de nombreuses enzymes différentes en raison de toutes ses activités et processus métaboliques complexes. Les enzymes servent de catalyseurs aux les diverses réactions chimiques métaboliques qui ont lieu, et une fois que l’enzyme est utilisée pour catalyser une réaction, elle disparaît, donc elle nécessite d’être remplacée.
Comment le pH affecte-t-il les réactions catalysées par les enzymes quizlet ?
A mesure que le pH augmente, l’activité de l’ enzyme augmente jusqu’à atteindre un point optimal dans lequel les enzymes se dénaturent et à mesure que le pH augmente, l’activité de l’ enzyme diminue. Ils peuvent également interagir avec le site actif et perturber la liaison hydrogène et la liaison aux résidus ioniques diminuant, ou dans certains cas augmentant, l’activité de l’ enzyme .
Que se passe-t-il pour la vitesse d’une réaction contrôlée par une enzyme lorsque le niveau de substrat est élevé ?
En augmentant la concentration de l’ enzyme , la vitesse maximale de la réaction augmente considérablement. Conclusions : Le taux d’une réaction chimique augmente lorsque la concentration en substrat augmente. Les Enzymes peuvent considérablement accélérer le taux d’une réaction . Cependant, les enzymes deviennent saturées lorsque la concentration du substrat est élevée .
Comment la concentration en substrat affecte-t-elle l’activité enzymatique ?
Concentration de substrat : L’augmentation de la concentration de substrat augmente également la vitesse de réaction jusqu’à un certain point. Une fois que toutes les enzymes se sont liées, toute augmentation du substrat n’aura aucun effet sur la vitesse de réaction, car les enzymes disponibles seront saturées et travailleront à leur vitesse maximale.
Comment appelle-t-on la combinaison d’une enzyme avec son substrat ?
Les enzymes se lient avec des réactifs chimiques appelés substrats . Les positions, séquences, structures et propriétés de ces résidus créent un environnement chimique très spécifique au sein du site actif. Un substrat chimique spécifique correspond à ce site comme une pièce de puzzle et rend l’ enzyme spécifique à son substrat .