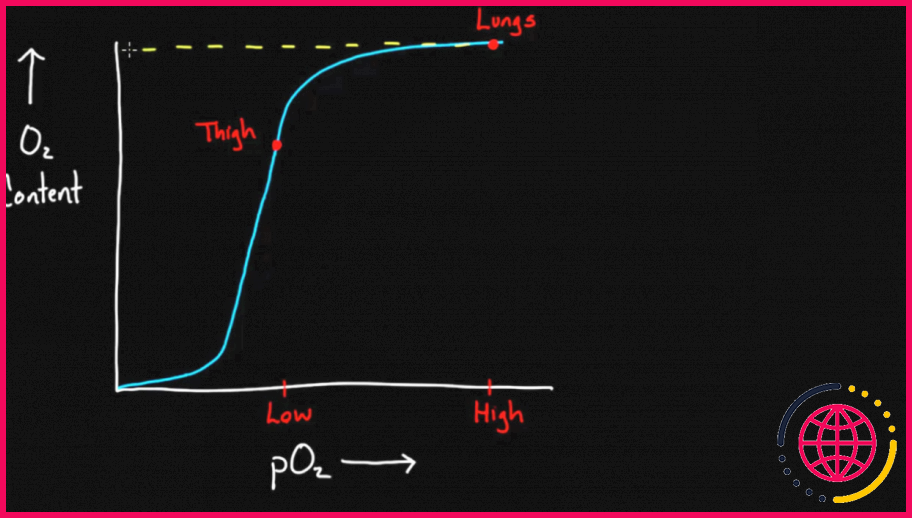
Qu’est-ce que l’hémoglobine à effet bohr ?
L’ effet Bohr a été découvert par un physiologiste Christian Bohr en 1904. Cet effet explique comment les ions hydrogène et le dioxyde de carbone affectent l’affinité de l’oxygène dans l’ Hémoglobine . Si le pH était plus bas qu’il ne l’était normalement (le pH physiologique normal est de 7,4), alors l’ hémoglobine ne fixe pas aussi bien l’oxygène.
A côté de cela, qu’est-ce que l’effet Bohr explique ?
Définition de l’ effet Bohr : la diminution de l’affinité pour l’oxygène d’un pigment respiratoire (comme l’hémoglobine) en réponse à une diminution du pH sanguin résultant d’une augmentation de la concentration de dioxyde de carbone dans le sang.
Par ailleurs, comment le pH affecte-t-il l’hémoglobine ? Transport de l’oxygène Lorsque le sang s’approche des poumons, la concentration en dioxyde de carbone diminue, ce qui entraîne une augmentation du pH . Cette augmentation de pH augmente l’affinité de l’ hémoglobine pour l’oxygène par l’effet Bohr, ce qui fait que l’ hémoglobine capte l’oxygène qui entre dans votre sang à partir de vos poumons afin de le transporter vers vos tissus.
Compte tenu de cela, qu’est-ce que l’effet Bohr et comment fonctionne-t-il ?
L’ effet Bohr décrit la capacité des globules rouges à s’adapter aux changements de l’environnement biochimique, en maximisant la capacité de liaison hémoglobine-oxygène dans les poumons tout en optimisant simultanément la livraison d’oxygène aux tissus ayant la plus grande demande.
Quelle est la différence entre l’effet Haldane et l’effet Bohr ?
L’inverse est également vrai : de faibles concentrations d’oxygène favorisent la charge du dioxyde de carbone sur l’hémoglobine. Dans les deux situations, c’est l’oxygène qui provoque la modification du taux de dioxyde de carbone. L’ effet Bohr , quant à lui, décrit comment le dioxyde de carbone et le H+ affectent l’affinité de l’hémoglobine pour l’oxygène.
Pourquoi l’effet Bohr est-il important ?
L’ effet Bohr permet une décharge accrue d’oxygène dans les tissus périphériques métaboliquement actifs tels que les muscles squelettiques en exercice. L’augmentation de l’activité des muscles squelettiques entraîne des augmentations localisées de la pression partielle du dioxyde de carbone, ce qui réduit à son tour le pH sanguin local.
Pourquoi la myoglobine ne présente-t-elle pas d’effet Bohr ?
L’ effet Bohr est la baisse de la saturation de l’hémoglobine qui se produit avec une diminution du pH et la liaison du CO2 aux groupes N- terminaux -NH2. La myoglobine ne présente pas d’effet Bohr car elle n’a pas de structure quaternaire pour réguler le degré de saturation par l’O2.
Où se produit l’effet Bohr ?
L’effet Bohr désigne la perte d’affinité pour l’O2 avec la diminution du pH (augmentation de l’acidité), comme se produit dans la microcirculation lorsque l’oxygène est consommé et que le CO2 (acide carbonique) est libéré par les tissus. Les protons déplacent l’équilibre vers la forme T en se liant aux acides aminés de surface.
Qu’est-ce que l’effet Haldane ?
L’effet Haldane effet est une propriété de l’hémoglobine décrite pour la première fois par John Scott Haldane. L’oxygénation du sang dans les poumons déplace le dioxyde de carbone de l’hémoglobine ce qui augmente l’élimination du dioxyde de carbone. Cette propriété est l’effet Haldane effet . Par conséquent, le sang oxygéné a une affinité réduite pour le dioxyde de carbone.
Quelle est la signification de la pCO2 ?
pression partielle du dioxyde de carbone.
Comment la température affecte-t-elle l’hémoglobine ?
Il s’avère que la température affecte l’affinité, ou la force de liaison, de l’ hémoglobine pour l’oxygène. Plus précisément, l’augmentation de la température diminue l’affinité de l’ hémoglobine pour l’oxygène. Lorsque l’oxyhémoglobine est exposée à des températures plus élevées dans les tissus en cours de métabolisation, l’affinité diminue et la hémoglobine se décharge de l’oxygène.
L’hémoglobine transporte-t-elle du co2 ?
Hémoglobine : La protéine à l’intérieur des globules rouges (a) qui transporte l’oxygène aux cellules et le dioxyde de carbone aux poumons est la hémoglobine (b). L’hémoglobine est constituée de quatre sous-unités symétriques et de quatre groupes hèmes. Cela s’explique par le fait que la molécule d’ hémoglobine change de forme, ou de conformation, lorsque l’oxygène se fixe.
Comment les 2/3 bpg affectent-ils l’hémoglobine ?
L’accumulation de 2 , 3 – BPG diminue l’affinité de l’ hémoglobine pour l’oxygène. Dans les tissus à forte demande énergétique, l’oxygène est rapidement consommé, ce qui augmente la concentration de H+ et de dioxyde de carbone. Grâce à l’ effet Bohr , la hémoglobine est incitée à libérer plus d’oxygène pour alimenter les cellules qui en ont besoin.
L’ajout de co2 à l’eau modifie-t-il le pH ?
Le dioxyde de carbone est la cause la plus courante de l’acidité de l’eau ¹5. Cependant, comme CO2
Les niveaux augmentent dans le monde, la quantité de CO2 dissous augmente également, et l’équation sera réalisée de gauche à droite. Cela augmente H2CO3, ce qui diminue pH .
Pourquoi l’hémoglobine libère-t-elle de l’oxygène ?
L’hémoglobine est contenue dans les globules rouges. L’hémoglobine libère l’ oxygène lié lorsque l’acide carbonique est présent, comme c’est le cas dans les tissus. Dans les capillaires, où le dioxyde de carbone est produit, l’ oxygène lié à l’ hémoglobine est libéré dans le plasma du sang et absorbé dans les tissus.
Où l’hémoglobine libère-t-elle l’oxygène ?
L’hémoglobine avec le dioxyde de carbone et les ions hydrogène liés est transportée dans le sang jusqu’aux poumons, où elle libère les ions hydrogène et le dioxyde de carbone et refixe l’ oxygène .
Quel devrait être votre taux d’hémoglobine ?
La fourchette normale pour l’ hémoglobine est : Pour les hommes, 13,5 à 17,5 grammes par décilitre. Pour les femmes, 12,0 à 15,5 grammes par décilitre.
Combien de molécules d’oxygène l’hémoglobine peut-elle transporter ?
quatre molécules d’oxygène
Qu’est-ce qui diminue l’affinité de l’hémoglobine pour l’oxygène ?
L’ affinité pour l’oxygène de l’ hémoglobine diminue à mesure que le pH décroit . Une fois qu’elle atteint le muscle, où le pH est plus faible, la baisse de l’ affinité pour l’oxygène permet à l’ hémoglobine de libérer son oxygène dans les tissus. Lorsque le dioxyde de carbone diffuse dans les globules rouges, sa dissociation provoque également une diminution du pH.
Comment fonctionne l’hémoglobine ?
Dans les poumons, où le taux d’oxygène est élevé, l’ hémoglobine se combine de manière lâche avec l’oxygène. La hémoglobine libère ensuite facilement cet oxygène dans les capillaires, où le taux d’oxygène est faible. Dans chaque molécule d’ hémoglobine , il y a quatre atomes de fer. Chaque atome de fer se lie à une molécule d’oxygène.
Comment le pCO2 affecte-t-il le pH ?
Tout changement dans le pCO2 aura un effet sur la réaction d’équilibre du CO2 et de H2O et affectera le pH . pO -pression partielle de l’oxygène. Acide respiratoire et acidose respiratoire–Le dioxyde de carbone est un « acide respiratoire » et est le seul acide qui peut être contrôlé par la respiration. Lorsque le pCO2 est élevé, il y a une acidose respiratoire.
Comment le co2 agit-il comme un acide ?
Le CO2 est la plus grande source d’ acide dans le corps car il se lie à H20 dans le sang et forme de l’ acide carbonique qui se dissocie ensuite en H+ et HCO3-.